¿La Suplementación con Creatina a Largo Plazo, Afecta la Función Renal de Individuos Entrenados en Fuerza, que Consumen una Dieta con Elevado Contenido de Proteínas?
Hamilton Roschel1,2,4, Rebeca Lugaresi1, Marco Leme1, Vítor de Salles Painelli1, Igor Hisashi Murai1, Marcelo Tatit Sapienza3, Antonio Herbert Lancha Junior1 y Bruno Gualano1,2
1School of Physical Education and Sport - Laboratory of Applied Nutrition and Metabolism. University of Sao Paulo, Av Mello de Moraes, 65, Sao Paulo, SP 05508-030, Brazil.
2School of Medicine – Division of Rheumatology. University of Sao Paulo, Av Mello de Moraes, 65, Sao Paulo, SP 05508-030, Brazil.
3School of Medicine – Division of Nuclear Medicine. University of Sao Paulo, Av Mello de Moraes, 65, Sao Paulo, SP 05508-030, Brazil.
4School of Physical Education and Sport - Laboratory of Neuromuscular Adaptations to Strength Training. University of Sao Paulo, Av Mello de Moraes, 65, Sao Paulo, SP 05508-030, Brazil.
Artículo publicado en el journal PubliCE, Volumen 0 del año 2013.
Publicado 12 de junio de 2013
Resumen
Registro del ensayo: ClinicalTrials.gov NCT01817673
Palabras clave: Tasa de filtración glomerular, clearance de 51Cr-EDTA, efectos secundarios
INTRODUCCION
La suplementación con creatina ha sido reconocida como uno de los suplementos dietéticos más eficaces, capaces de incrementar la fuerza muscular y la masa magra [1], así como también el rendimiento de ejercicios de alta intensidad [2]. Sin embargo, el uso indiscriminado de este suplemento ha planteado preocupaciones sobre su seguridad, especialmente con respecto al funcionamiento de los riñones [3].
A pesar del número creciente de publicaciones que muestran que la suplementación con creatina no afectaría el funcionamiento de los riñones en los seres humanos [4-10], se ha recomendado analizar con más detalle los efectos crónicos de la suplementación con creatina en algunas poblaciones específicas [3]. En este sentido, hay una afirmación empírica que los suplementos con creatina podrían significar un riesgo para quienes consumen proteínas en exceso. De hecho, hay evidencia convincente que indica que las dietas con elevado contenido de proteínas pueden acelerar el deterioro renal en individuos con enfermedades renales crónicas [11], aunque no se sabe si esto también se produce en personas saludables [12].
Los sujetos entrenados en fuerza consumen a menudo una dieta con elevado contenido de proteínas junto con suplementos de creatina, con el objetivo de aumentar la potencia/fuerza y masa magra. La supuesta "carga excesiva del riñón" causada por la creatina (y su derivado la creatinina) y la ingesta excesiva de proteínas ameritan una extensa investigación. Por consiguiente, el propósito de este estudio fue examinar los efectos de la suplementación con creatina sobre el funcionamiento de los riñones en individuos entrenados en fuerza, que consumen una dieta con elevado contenido de proteínas. En la mayoría de los estudios previos realizados sobre suplementación con creatina en seres humanos, se evaluó la función de los riñones a través de la creatinina sérica o sus ecuaciones derivadas. Sin embargo, la conversión espontánea de creatina en creatinina [13] puede sugerir falsamente que existe una disminución en el funcionamiento de los riñones en individuos que consumen un suplemento con creatina [8]. Para superar esta desventaja potencial, en este estudio nosotros usamos la metodología de referencia para medir la tasa de filtración glomerular de manera precisa; el clearance de 51Cromo-Acidoetilendiaminotetraacético (51Cr-EDTA).
METODOS
Sujetos
En este estudio se seleccionaron varones jóvenes saludables que se encontraban realizando entrenamiento de fuerza regularmente desde hacía por lo menos 1 año, y que consumían una dieta con elevado contenido de proteínas (≥1,2 g/kg/d; que es una prescripción usual en sujetos entrenados en fuerza [14]). El criterio de exclusión incluyó: dieta vegetariana, uso de suplementos de creatina en los últimos 6 meses, enfermedad renal crónica y consumo de esteroides anabólicos. Se solicitó a los participantes que mantuvieran su dieta habitual. Las características de los participantes se presentan en la Tabla 1. El estudio fue aceptado por el Comité Asesor de Ética de la Escuela de Educación Física y Deporte de la Universidad de Sao Paulo. Todos los participantes firmaron un consentimiento informado. Este ensayo fue registrado en clinicaltrials.gov como NCT01817673.
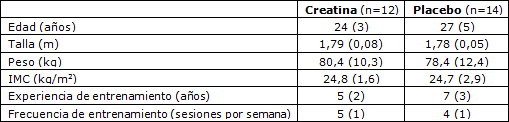
Tabla 1. Características de los participantes. Los datos se expresan en forma de media (desviación estándar). IMC = Índice de masa corporal
Protocolo experimental
El estudio de 12 semanas, aleatorizado, doble-ciego y controlado con placebo, fue realizado entre julio de 2011 y febrero de 2013 en Sao Paulo, Brasil. Los participantes fueron asignados a un grupo que consumió creatina o a un grupo que consumió un placebo siguiendo una aleatorización en doble ciego. Todos los participantes continuaron con sus rutinas de entrenamiento de resistencia habitual durante el estudio. Los participantes fueron evaluados al inicio del estudio (Pre) y después de 12 semanas (Post). La determinación del clearance de 51Cr-EDTA se realizó para medir la tasa de filtración glomerular. Adicionalmente, se obtuvieron muestras de sangre y se recolectó la orina de 24 horas luego de un ayuno de 12 hs para evaluar el funcionamiento de los riñones. Se solicitó a los participantes que no realizaran actividad física extenuante en las 24 hs previas a las evaluaciones Pre y Post. La ingesta de alimentos se evaluó por registros de comidas de 7 días. Este método consiste en anotar los alimentos y las bebidas consumidos durante 7 días consecutivos. La energía y los macronutrientes fueron analizados con el software Dietpro® 5i (Sao Paulo, Brasil).
Protocolo de suplementación con creatina y procedimiento de enmascaramiento.
El grupo creatina recibió monohidrato de creatina (dosis de 20 g/d durante 5 días y luego dosis de 5 g/d a lo largo del tratamiento). El grupo placebo recibió la misma dosis de dextrosa. Se aconsejó a los participantes que consumieran sus suplementos preferentemente junto con las comidas (ej., desayuno, almuerzo, media tarde y cena). Los paquetes de los suplementos estaban codificados para que ni los investigadores ni los participantes supieran cual era el contenido hasta que se completaran los análisis. Para verificar la pureza de la creatina usada, se analizó una muestra por cromatografía líquida de alta eficacia (HPLC). Esto estableció un 99,9% de pureza, y no se observaron otros picos en el cromatograma (creatinina, diciandiamida, y ciclo creatina <0,01%).
Clearance (depuración) de 51Cr-EDTA
Después de una dieta de 24 horas restringida en proteínas y de un ayuno de toda la noche de 12 horas, los participantes arribaron al centro de investigación clínica a las 7:00 de la mañana, y descansaron en posición supina con un catéter permanente de polietileno insertado en la vena cubital en ambos brazos. Una sola dosis de 3,7MBq (100 µCi) del marcador radioactivo 51Cr-EDTA, en un volumen de 1 ml, se inyectó intravenosamente en el brazo derecho. El catéter había sido enrasado con 10 ml de solución salina. Se extrajeron muestras de sangre de 10-ml en tubos heparinizados en intervalos precisamente medidos del brazo contrario a las 4 horas y 6 horas después de la inyección. La curva de desaparición en plasma fue trazada con los resultados de estos puntos de muestreo. Para medir la actividad del radioisótopo, las muestras de sangre fueron centrifugadas a 1500 g durante 10 min y para determinar la energía de cromo-51 (320 keV), 3 ml de plasma fueron medidos en un contador correctamente calibrado (Genesys GeniiTM, LabLogic Systems Inc, Brandon, Florida, USA). Todas las muestras, incluyendo una muestra de 3 ml de solución estándar tomada como un alícuota de 3,7MBq (100 µCi) 51Cr-EDTA diluidos hasta 500 mL de solución salina, fueron analizadas en el contador durante 5 min. El clearance plasmático se calculó por el método de pendiente intersección con un modelo de un solo compartimiento, el cual asume que el marcador se disemina en su volumen de distribución inmediatamente después de la inyección. El método de Brochner-Mortensen se usó para corregir los errores sistemáticos de la técnica pendiente intersección según la siguiente ecuación:
Clc = 0,9908 x Clnc- 0,001218 x Clnc2
donde Clc es el clearance corregido para el primer exponencial y Clnc es el clearance no corregido. Los errores sistemáticos causados por una distribución anormal del radioisótopo se corrigieron con el método de Groth. El clearance de 51Cr-EDTA también se corrigió para un área de superficie corporal de 1,73 m2. El coeficiente de variación (CV) para el clearance de 51Cr-EDTA era 9,7%.
Análisis de sangre y de orina.
Las muestras de sangre se obtuvieron de la vena antecubital, luego de un ayuno nocturno de 12 horas. Los participantes mantuvieron su dieta normal durante las 24 horas en que se realizó la recolección de orina. Las muestras de orina se guardaron a aproximadamente 4°C. Las determinaciones efectuadas en sangre y orina se realizaron por la mañana. La creatinina se determinó con el método cinético de Jaffe. El contenido de sodio y potasio en orina y en suero fue determinado mediante un fotómetro de llama (FP8800, Kruss®, Hamburgo, Alemania). La urea fue determinada por medio del método cinético-UV. La albuminuria fue determinada por nefelometría y la proteinuria a través del método de cloruro de benzetonio.
Todas las muestras fueron analizadas por duplicado y los CV para creatinina sérica, sodio sérico, potasio sérico, urea sérica, proteinuria, albuminuria, sodio urinario, y el potasio urinario, fueron 2,0, 2,2, 1,1, 2,1, 2,3, 5,3, 24,5 y 16,4% respectivamente.
Análisis estadístico
Se determinó que se necesitaban 24 participantes para obtener una potencia de 80% (significancia de 5%, a dos colas) para detectar una reducción de 20% en el clearance de 51Cr-EDTA. Para tener en cuenta los abandonos de los participantes a mitad del tratamiento, nosotros ampliamos nuestro tamaño de muestra de estudio a 46 participantes.
Los datos fueron evaluados mediante un Modelo Mixto con ajuste de Kenward-Roger para grupos de tamaños dispares, usando el software SAS 9.2 (Instituto SAS Inc., Cary, NC, EE.UU.). Grupo (creatina y placebo) y tiempo (Pre y Post) fueron considerados como factores fijos y los participantes fueron definidos como factor aleatorio. Se estableció que se utilizaría el test post hoc de Tukey ajustado, en aquellos casos en que se obtuviera un F con valor significativo. La diferencia entre grupos en la proporción de participantes que presentaban disminución en el clearance de 51Cr-EDTA se analizó con el test de Chi-cuadrado (X2). El nivel de significancia fue fijado en p <0,05. Los datos se presentan en forma de media y desviación estándar.
RESULTADOS
Flujo de participantes
El flujo de participantes se presenta en la Figura 1. Un total de 115 voluntarios fueron evaluados para poder participar y 69 voluntarios no cumplieron con el criterio de inclusión. Los 46 participantes restantes fueron asignados al azar al grupo que consumió creatina (n = 23) o al grupo que consumió el placebo (n = 23). Posteriormente, 15 participantes abandonaron el estudio por razones personales (8 del grupo creatina y 7 del grupo placebo). Adicionalmente, 5 participantes (3 del grupo creatina y 2 del grupo placebo) no asistieron a la valoración post intervención; por lo tanto no fueron considerados en el análisis. Por lo tanto, el análisis se realizó con 12 participantes en el grupo creatina y 14 participantes en el grupo placebo (n = 26).
Ingesta de alimentos
La Tabla 2 muestra los datos correspondientes a la ingesta de alimentos. La ingesta de proteínas varió de 1,2 a 3,1 g/kg/d. La dieta se mantuvo sin cambios a lo largo del estudio.
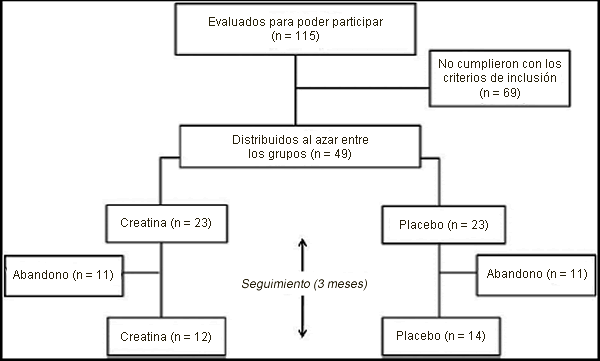
Figura 1. Diagrama de flujo de los participantes.
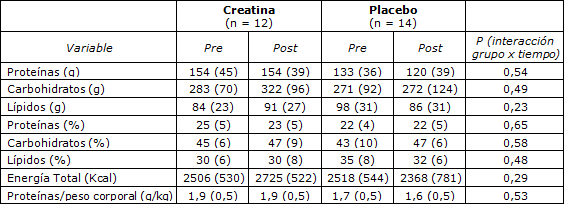
Tabla 2. Ingesta de alimentos antes (Pre) y después de 12 semanas (Post) de la suplementación con creatina o placebo, en individuos entrenados en fuerza que consumen una dieta con elevado contenido de proteínas. Los datos se expresan en forma de media (desviación estándar). No se observaron diferencias entre los grupos al inicio del estudio. No se observaron diferencias dentro de los grupos ni entre los grupos.
Valoraciones de la función renal
La Figura 2 presenta los datos del clearance de 51Cr-EDTA. No se observaron diferencias significativas entre los grupos en Pre o Post (interacción grupo x tiempo: F = 0,21, p = 0,64). En el grupo creatina, 2 de 12 participantes presentaron una disminución en el clearance de 51Cr-EDTA, mientras que en el grupo placebo 6 de 14 participantes experimentaron una reducción en el clearance de Cr-EDTA (P (X2> 2,081) = 0,149).
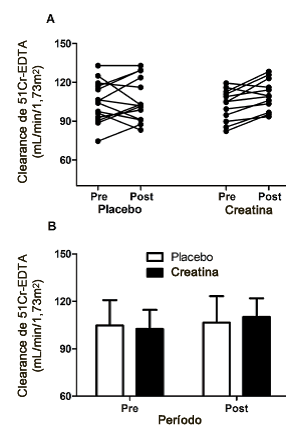
Figura 2. Clearance de 51Cr-EDTA antes (Pre) y después de 12 semanas (Post) del tratamiento de suplementación ya sea con creatina (n = 12) o con placebo (n = 14) en individuos entrenados en fuerza que consumen una dieta con elevado contenido de proteínas. Panel A: Datos individuales. Panel B: Valores de media ± desviación estándar. No se observaron diferencias significativas entre los grupos a lo largo del tiempo (interacción grupo x tiempo) (F = 0,21, p = 0,64). Nota: factores de conversión para unidades: tasa de filtración de glomerular en mL/min/1,73m2 a mL/s/1,73m2, × 0,01667.
La Tabla 3 presenta los datos de albuminuria, proteinuria, contenido sérico y urinario de sodio y potasio, urea sérica y creatinina sérica. No se observaron diferencias significativas entre los grupos en ninguno de los parámetros (p> 0,05). Ninguno de los participantes presentó albuminuria o proteinuria.
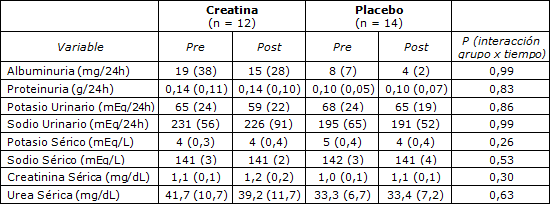
Tabla 3. Parámetros correspondientes al funcionamiento renal antes (Pre) y después de 12 semanas (Post) de la suplementación con creatina o con placebo en individuos entrenados en resistencia que consumen una dieta con elevado contenido de proteínas.
Los datos se expresan en forma de media (desviación estándar). No se observaron diferencias significativas entre los grupos al inicio del estudio. No se observaron diferencias significativas ni dentro de los grupos ni entre los grupos. Nota: factores de conversión para unidades: Creatinina sérica en mg/dL a mol/L x 88,4; Urea sérica en mg/dL a mmol/L, x 0,166; tasa de filtración de glomerular en mL/min/1,73 m2 a mL/s/1,73m2, × 0,01667.
DISCUSIÓN
Los resultados presentes coinciden con lo observado en otras investigaciones que han demostrado la seguridad de la suplementación con creatina para la función de los riñones en distintas poblaciones [4-9]. Sin embargo, la mayoría de estos estudios estimó la tasa de filtración glomerular usando los marcadores endógenos séricos que se usan ampliamente en la práctica clínica, pero que son potencialmente susceptibles a errores metodológicos. Por ejemplo, la creatinina sérica y sus ecuaciones derivadas son influenciadas por la ingesta dietética, particularmente por los alimentos o suplementos que contienen creatina. Luego de la ingesta de creatina, poGenesys GeniiTM, LabLogic Systems Incdríamos esperar un aumento en la creatinina sérica, debido a que la creatina se convierte espontánea e irreversiblemente en creatinina. Por lo tanto, cuando sólo se tienen en cuenta datos de creatinina sérica, se puede obtener un diagnóstico falso positivo de una función renal disminuida en un individuo que consume un suplemento con creatina. Aunque el contenido de creatinina sérica no se elevó significativamente en el presente estudio, las observaciones anteriores de nuestro grupo [8] y de otros grupos [15] apoyan la inexactitud de los marcadores basados en la creatinina para la evaluación de la función renal, en individuos que reciben un suplemento con creatina. Para evitar este sesgo potencial, medimos la tasa de filtración de glomerular utilizando la metodología de referencia del clearance de 51Cr-EDTA, que nos permitió concluir adecuadamente que, en este estudio, la suplementación con creatina no afectó la función renal.
Previamente, aplicando la técnica mencionada anteriormente, demostramos que 35 días de suplementación con creatina no alteraron la función de los riñones en un hombre de 20 años que tenía un solo riñón [16]. Más aún, nosotros informamos que 3 meses de suplementación con creatina no tuvieron un efecto perjudicial en el funcionamiento de los riñones en mujeres post menopáusicas [9] y en pacientes con diabetes de tipo 2 [17], lo que corrobora la seguridad de este suplemento. Los datos presentes extienden esta noción a los consumidores de creatina típicos, lo que sugiere que los individuos saludables entrenados en fuerza pueden “lidiar” con la suplementación con creatina aún en combinación con un nivel más alto de ingesta de proteínas (considerado la Ingesta Dietética Recomendada (RDI) de 0,8 g/kg/d). En consonancia con nuestros resultados, algunos estudios transversales no observaron diferencias significativas en la función de los riñones entre consumidores de elevada cantidad de proteínas y consumidores de bajo contenido de proteínas [18,19]. De hecho, dada la habituación del ser humano a una dieta con elevado contenido de nitrógeno a lo largo de la evolución, estos resultados no deberían ser considerados como inesperados. Sin embargo, estudios prospectivos adicionales deberían analizar el impacto de dietas crónicas con elevado contenido de nitrógeno sobre la función de los riñones en individuos saludables.
Este estudio no carece de limitaciones. Primero, el seguimiento de este estudio es demasiado corto, lo que impide obtener cualquier conclusión definitiva. Originalmente, este ensayo fue diseñado para cubrir un período de 12 meses. Sin embargo, una tasa de abandono drástica nos obligó a reducir el período de seguimiento. Por consiguiente, es necesario realizar pruebas con tratamientos de mayor duración. Segundo, seleccionamos a los participantes entrenados recreacionalmente para aumentar la validez ecológica de este estudio, dado que se piensa que esta población es la principal consumidora de suplementos de creatina. Sin embargo, es posible que los atletas altamente entrenados que consumen esteroides anabólicos y que se encuentran bajo regímenes de entrenamiento de fuerza exhaustivos puedan experimentar una respuesta diferente frente a la suplementación con creatina. Finalmente, debemos destacar que todos los individuos eran aparentemente saludables, por lo que estos datos no pueden ser extrapolados a los individuos con, o en riesgo de sufrir, enfermedades renales crónicas. En tales condiciones, la función renal de los consumidores de creatina debe ser supervisada sistemáticamente.
CONCLUSIONES
Tres meses de suplementación con creatina no ejercen un efecto perjudicial en la función de los riñones en sujetos entrenados en fuerza que consumen una dieta con elevado contenido de proteínas (es decir, ≥ 1,2 g/kg/d).
Abreviaturas
Cr-EDTA: 51Cromo-ácidoetilendiaminotetraacético; Pre: Inicio del estudio; Post: después de 12 semanas; CV: coeficiente de variación; IMC: índice de masa corporal; RDI: Ingesta Dietética Recomendada,; X2: Test Chi-cuadrado,
Intereses de competencia
Los autores declaran que no poseen ningún conflicto de interés.
Contribuciones de los autores
RL y BG fueron los principales redactores del manuscrito; ML, HR, MTS, y AHLJ fueron los principales revisores del manuscrito; BG, HR, y AHLJ participaron en el concepto y diseño; RL, ML, VSP, y MTS fueron los responsables de la adquisición de los datos; BG, HR, VSP, y RL participaron en el análisis y en la interpretación de los datos. Todos los autores leyeron y aprobaron el manuscrito final.
AGRADECIMIENTOS
Agradecemos a Fundação de Amparo à Pesquisa do Estado de São Paulo y al Conselho Nacional de Desenvolvimento Científico e Tecnológico por el apoyo financiero.
Referencias
1. Gualano B, Roschel H, Lancha-Jr AH, Brightbill CE, Rawson ES (2012). In sickness and in health: The widespread application of creatine supplementation. Amino Acids, 43:519–529
2. Buford TW, Kreider RB, Stout JR, Greenwood M, Campbell B, Spano M, Ziegenfuss T, Lopez H, Landis J, Antonio J (2007). International Society of Sports Nutrition position stand: creatine supplementation and exercise. J Int Soc Sports Nutr, 4:6
3. Kim HJ, Kim CK, Carpentier A, Poortmans JR (2011). Studies on the safety of creatine supplementation. Amino Acids, 40:1409–1418
4. Poortmans JR, Auquier H, Renaut V, Durussel A, Saugy M, Brisson GR (1997). Effect of short-term creatine supplementation on renal responses in men. Eur J Appl Physiol Occup Physiol, 76:566–567
5. Poortmans JR, Francaux M (1999). Long-term oral creatine supplementation does not impair renal function in healthy athletes. Med Sci Sports Exerc, 31:1108–1110
6. Poortmans JR, Kumps A, Duez P, Fofonka A, Carpentier A, Francaux M (2005). Effect of oral creatine supplementation on urinary methylamine, formaldehyde, and formate. Med Sci Sports Exerc, 37:1717–1720
7. Gualano B, de Salles PV, Roschel H, Lugaresi R, Dorea E, Artioli GG, Lima FR, da Silva ME, Cunha MR, Seguro AC, Otaduy MC, Shimizu MH, Sapienza MT, da Costa LC, Bonfá E, Lancha Junior AH (2011). Creatine supplementation does not impair kidney function in type 2 diabetic patients: A randomized, double-blind, placebo-controlled, clinical trial. Eur J Appl Physiol, 111:749–756
8. Gualano B, Ugrinowitsch C, Novaes RB, Artioli GG, Shimizu MH, Seguro AC, Harris RC, Lancha AH Jr (2008). Effects of creatine supplementation on renal function: A randomized, double-blind, placebo-controlled clinical trial. Eur J Appl Physiol, 103:33–40
9. Neves M Jr, Gualano B, Roschel H, Lima FR, Lúcia De Sá-Pinto A, Seguro AC, Shimizu MH, Sapienza MT, Fuller R, Lancha AH Jr, Bonfa E (2011). Effect of creatine supplementation on measured glomerular filtration rate in postmenopausal women. Appl Physiol Nutr Metab, 36:419–422
10. Kreider RB, Melton C, Rasmussen CJ, Greenwood M, Lancaster S, Cantler EC, Milnor P, Almada AL (2003). Long-term creatine supplementation does not significantly affect clinical markers of health in athletes. Mol Cell Biochem, 244:95–104
11. Bernstein AM, Treyzon L, Li Z (2007). Are high-protein, vegetable-based diets safe for kidney function? A review of the literature. J Am Diet Assoc, 107:644–650
12. Lowery LM, Devia L (2009). Dietary protein safety and resistance exercise: What do we really know? . J Int Soc Sports Nutr, 6:3
13. Wyss M, Kaddurah-Daouk R (2000). Creatine and creatinine metabolism. Physiol Rev, 80:1107–1213
14. Burd NA, Tang JE, Moore DR, Phillips SM (2009). Exercise training and protein metabolism: Influences of contraction, protein intake, and sex-based differences. J Appl Physiol, 106:1692–1701
15. Refaie R, Moochhala SH, Kanagasundaram NS (2007). How we estimate gfr–a pitfall of using a serum creatinine-based formula. Clin Nephrol, 68:235–237
16. Gualano B, Ferreira DC, Sapienza MT, Seguro AC, Lancha AH Jr (2009). Effect of short-term, high-dose creatine supplementation on measured GFR in a young man with a single kidney. Am J Kidney Dis, 55:e7–e9
17. Gualano B, de Salles PV, Roschel H, Artioli GG, Neves M Jr, de Sá Pinto AL, da Silva ME, Cunha MR, Otaduy MC, Leite Cda C, Ferreira JC, Pereira RM, Brum PC, Bonfá E, Lancha AH Jr: Creatine in type 2 d (2011). A randomized, double-blind, placebo-controlled trial. Med Sci Sports Exerc, 43:770–778
18. Poortmans JR, Dellalieux O (2000). Do regular high protein diets have potential health risks on kidney function in athletes?. Int J Sport Nutr Exerc Metab, 10:28–38
19. Brândle E, Sieberth HG, Hautmann RE (1996). Effect of chronic dietary protein intake on the renal function in healthy subjects. Eur J Clin Nutr, 50:734–740