Rehabilitación del paciente cardíaco en el siglo XXI: Cambiando paradigmas y percepciones
Barry A Franklin1, Kimberly Bonzheim1 y Seynour Gordon1
Departamento de Medicina, División de Cardiología (Rehabilitación Cardíaca), William Beaumont Hospital, Royal Oak, Michigan, E.E.U.U.
Artículo publicado en el journal PubliCE, Volumen 0 del año 1998.
Publicado 1 de diciembre de 2003
Resumen
Palabras clave: rehabilitación cardíaca, prevención secundaria, lípidos, lipoproteínas
INTRODUCCION
La ateroesclerosis coronaria comprende una acumulación localizada de lípidos y tejido fibroso dentro de la arteria coronaria, que progresivamente estrechan el lumen del vaso. Los filamentos de grasa pueden progresar con el tiempo y llegar a placas fibrosas y eventualmente a formar un ateroma. El flujo sanguíneo coronario normalmente no se ve significativamente comprometido hasta que la obstrucción alcanza el 75% del área transversal del vaso. No obstante, lesiones que están menos obstruidas podrían aún así complicarse por hemorragias, ruptura de placas, o trombosis, llevando a angina de pecho, infarto de miocardio (IM), o muerte súbita cardiaca, independientemente de si el tratamiento consiste en agentes antianginosos, revascularización coronaria, o ambos. Afortunadamente, la cardiología moderna ha hecho grandes mejorías en el tratamiento de pacientes con enfermedades cardiacas, y los avances en rehabilitación son parcialmente responsables de esta situación.
En este artículo se hace una revisión de los paradigmas y percepciones en cuanto a la rehabilitación de pacientes con enfermedades cardiacas, con referencia específica a las estrategias de tratamiento e intervenciones, relajación de la restricción de la actividad inmediatamente después de un evento coronario agudo, recomendaciones de ejercicio y consideraciones asociadas con respecto a la seguridad, temas vocacionales, y el armamento actual de terapias de reducción de riesgos.
TENDENCIAS RECIENTES EN EL TRATAMIENTO DE PACIENTES CON ENFERMEDADES CARDIACAS
Los individuos que experimentan un evento coronario agudo tienen un mayor riesgo de eventos posteriores, independientemente del tratamiento. El mayor número de pacientes que se somete a reiteradas angioplastias coronarias transluminales percutáneas (PTCA) y/o a cirugías de by-pass en las arterias coronarias (CABGS) confirma la naturaleza paliativa de la mayoría de los procedimientos de revascularización coronaria. Sin embargo, la minuciosa descripción de la estratificación de los riesgos ha ayudado a delinear aquellos pacientes que más se beneficiarían con estudios diagnósticos adicionales y/o con las intervenciones referidas anteriormente, incluyendo los servicios de rehabilitación cardiaca.
Estratificación de riesgos
La identificación de pacientes apenas después de un infarto agudo de miocardio que están en mayor riesgo de eventos cardíacos posteriores ofrece los beneficios importantes: los pacientes con riesgo moderado a alto pueden ser evaluados para una terapia medicamentosa más intensiva, caterización cardiaca intervencionista, o cirugía; y, los pacientes con bajo riesgo pueden evitar la caterización cardiaca inmediata y la restricción injustificada de sus actividades laborales y recreativas.
DeBusk y colegas (1986) enfatizaron en su algoritmo de estratificación de riesgos que es el grado de disfunción del ventrículo izquierdo o la isquemia miocárdica residual en reposo, o inducida por el ejercicio, los que determinan el riesgo de futuros eventos cardiacos. Esta última, resultante del compromiso coronario residual, podría manifestarse como angina de pecho, depresión isquémica del segmento ST (≥ 1 mm), o anormalidades transitorias en la perfusión cuando el test convencional de esfuerzo es combinado con centellografía que emplea Cloruro de Talio-201 o Tecnecio Tc-99 (Cardiolite).
Aproximadamente, la mitad de los que sobreviven a un infarto agudo de miocardio tienen un daño cardíaco mínimo y no evidencian isquemia miocárdica residual. Este grupo está en un bajo riesgo de muerte con una tasa de mortalidad en el primer año menor al 2%. De los pacientes restantes, aproximadamente el 30% presenta isquemia inducida por el ejercicio, lo que significa más miocardio en peligro, y el 20% tiene evidencias clínicas de disfunciones severas en el ventrículo izquierdo. Estos son los grupos con riesgos moderados y altos, con tasas asociadas de mortalidad en el primer año de 10 a 25% y >25%, respectivamente.
Opciones de tratamiento
A pesar de que el grado de disfunción ventricular izquierda y la isquemia miocárdica residual determinan en gran parte el riesgo de futuros eventos cardiacos, el nivel de riesgo puede influirse a través de numerosas intervenciones y cambios en el estilo de vida (Figura 1). Las series multicéntricas han confirmado que la mortalidad a partir de un IM puede disminuirse aproximadamente en un 25% con una reperfusión trombolítica precoz (Simoons y cols., 1986), PTCA emergente (Grines y cols., 1993), o con ambos. Los pacientes con riesgo moderado podrían experimentar una reducción en los síntomas anginosos y en los eventos cardiacos recurrentes a partir de una PTCA o un CABGS. Las intervenciones agresivas sobre los factores de riesgo dirigidas a dejar de fumar y reducción del colesterol; y las drogas eficaces, incluyendo beta-bloqueantes, aspirina, u otros agentes activos en las plaquetas, los inhibidores de la enzima de conversión de la angiotensina, y los agentes de disminución de lípidos, han producido una regresión en el desarrollo de la ateroesclerosis coronaria documentada angiográficamente y/o reducciones significativas en la morbi-mortalidad relacionada con las enfermedades cardiovasculares (Ornish y cols., 1990; Haskell y cols., 1994; Gould y cols., 1995). Además, se ha mostrado que la suplementación con vitamina B, especialmente ácido fólico, reduce los niveles elevados de homocisteína en sangre (> o igual a 13 micromoles/lt.), los cuales están fuertemente asociados a un mayor riesgo de enfermedades en las arterias coronarias (CAD) (Boushey y cols., 1995). Los meta-análisis de los estudios clínicos controlados y randomizados (al azar), llevados a cabo al comienzo de los ‘80 con pacientes post-IM, mostraron que la rehabilitación cardiaca basada en el ejercicio disminuye entre un 20 y un 24% la mortalidad relacionada con enfermedades cardiovasculares y con todas las causas (Tabla 1) (Oldridge y cols., 1988; O'Connor y cols., 1989; Lau y cols., 1992), especialmente como componente de la rehabilitación multifactorial (por ej., 26% de reducción en la mortalidad vs. el 15% en los trabajos sólo con ejercicio) (Wenger y cols., 1995), sin diferencia en la tasa de eventos cardíacos recurrentes no fatales. Sin embargo, los actuales procedimientos trombolíticos y de revascularización, los cuales reducen marcadamente la mortalidad precoz post-infarto, podrían disminuir el impacto de los programas de rehabilitación cardiaca sobre la supervivencia. Por otro lado, el tiempo (progresión de la enfermedad), la inadecuada adherencia del paciente al tratamiento, y las disfunciones psicológicas, manifestadas como ira, depresión, hostilidad y/o aislamiento social (Williams y cols., 1992), pueden llevar a un aumento en el riesgo y a un pronóstico adverso.

Figura 1. Variables que podrían influir potencialmente en el nivel de
riesgo del paciente (PTCA=angioplastia coronaria transluminal percutánea;
CABGS= cirugía de injerto por by-pass en las arterias coronarias).
(*) Basado en el grado de isquemia miocárdica y disfunción del VI.
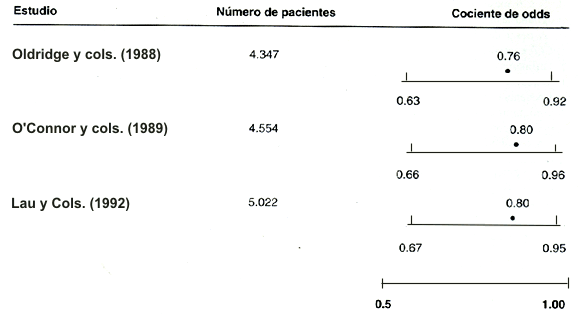
Tabla 1. Meta-análisis de los efectos de la rehabilitación cardiaca basada
en el ejercicio sobre la mortalidad de todas las causas, luego de un infarto
agudo de miocardio.
Aparición emergente de la rehabilitación cardiaca
Dentro de la Organización Mundial para la Salud, el Comité de Expertos sobre la Rehabilitación de Pacientes con Enfermedades Cardiovasculares (1964) definió a la rehabilitación cardiaca como las "intervenciones tendientes a acompañar las actividades necesarias para asegurar a los pacientes las mejores condiciones físicas, mentales, y sociales de manera que puedan, por sus propios medios, reanudar y mantener de la manera más normal posible su lugar en la comunidad". Recientemente, el Comité (1993) redefinió los objetivos de la rehabilitación cardiaca, considerada a "mejorar la capacidad funcional, aliviar o disminuir los síntomas relacionados con la actividad, reducir la invalidez, y permitir al paciente cardíaco volver al rol útil y personalmente gratificante que tenía en la sociedad".
Los programas de rehabilitación cardiaca, por lo general, están basados en un accionar continuo de 3 o 4 fases: * Fase 1: período de convalecencia en el hospital, el cual ha disminuido notablemente en los últimos años (generalmente de 4 a 7 días para pacientes con un infarto agudo de miocardio o luego de un by-pass (CABGS)); * Fase II: etapa inicial luego del alta hospitalaria (ordinariamente hasta 12 semanas para pacientes seleccionados); * Fase III: supone un programa supervisado más prolongado (usualmente de 3 a 6 meses o más de duración); * Fase IV: programa de mantenimiento (de duración indefinida).
A pesar de que el control electrocardiográfico (ECG) continuo fue ampliamente utilizado durante los primeros años de rehabilitación en la Fase II, los estudios recientes sugieren que no hay diferencias en la frecuencia de complicaciones cardiovasculares en los programas con y sin ECG (Van Camp y Peterson, 1986). En consecuencia, el costoso monitoreo continuo, actualmente se recomienda sólo para pacientes con riesgo moderado a alto.
Los objetivos de la rehabilitación cardiaca contemporánea son incrementar la capacidad funcional, disminuir los síntomas, abandonar el cigarrillo, modificar los perfiles de lípidos y lipoproteínas, disminuir el peso corporal y las reservas de grasas, reducir la presión sanguínea, y mejorar el bienestar psico-social. Son de capital importancia las intervenciones diseñadas a retardar la progresión, promover la estabilidad plaquetaria, o inducir la regresión de los procesos ateroescleróticos subyacentes, y a restaurar y mantener el óptimo funcionamiento físico, psico-social, emocional, y vocacional. De acuerdo a estos objetivos, los programas abarcativos y multidisciplinarios deberían incluir cuatro componentes principales: entrenamiento físico, modificación de los factores de riesgo, apoyo médico y de emergencias, y ayuda psico-social/vocacional (Figura 2).
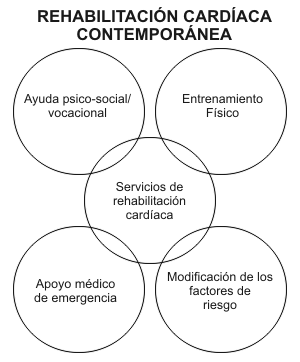
Figura 2. Componentes claves de un programa de rehabilitación para
pacientes con enfermedades cardíacas.
La rehabilitación cardiaca basada en el ejercicio se ha vuelto ahora el "criterio de cuidado" dentro de la comunidad médica por la cual un amplio espectro de pacientes son reestablecidos a su óptimo estado físico, médico, y psico-social luego de un evento cardiaco agudo (Franklin, 1991). En los programas de rehabilitación están incluidos los pacientes de siempre: IM, CABGS y PTCA, y además, los siguientes casos: pacientes coronarios con o sin isquemia miocárdica residual, fallas cardíacas compensadas, miocardiopatías, y arritmias ventriculares aberrantes; distintas categorías de pacientes con enfermedad cardiaca no isquémica; pacientes con enfermedad pulmonar concomitante; pacientes que se han sometido a un implante de marcapaso o cardiovertor-defibrilador, reparación o reemplazo de válvulas cardíacas, y trasplantes de corazón; pacientes añosos; y pacientes médicamente complejos y que están bajo múltiples medicamentos.
"LIBERALIZACIÓN" DE LA ACTIVIDAD EN EL TRATAMIENTO DEL PACIENTE CON INFARTO AGUDO DE MIOCARDIO
A pesar de que en su texto de Cardiología, Friedberg (1966) aún recomendaba de 2 a 3 semanas de reposo en cama y un período adicional de 3 a 4 semanas en el hospital para el paciente con IM agudo, el reposo prolongado en cama ya casi no se usa para ningún paciente con enfermedades en las arterias coronarias debido a un acortamiento extraordinario en la estadía hospitalaria. Además, se ha demostrado que guardar reposo durante mucho tiempo produce un desacondicionamiento fisiológico y una disminución significativa en el máximo consumo de oxígeno (VO2 máx.) y otras secuelas adversas incluyendo: atrofia muscular, debilitamiento, constipación, retención urinaria, tromboflebitis, embolia pulmonar, neumonía hipostática, intolerancia ortostática, y depresión (Winslow, 1985). En un tratado con amplias referencias, Asher (1947) describió los "peligros de ir a la cama".
"Miren al paciente acostado en la cama. Qué imagen patética que dá!. La sangre coagulando en sus venas, el calcio vaciándose de sus huesos, las heces acumulándose en su colon, la carne pudriéndose en su sillón, la orina escapándose de su vejiga distendida, y el espíritu evaporándose de su alma".
Harrison (1944) sugirió que el reposo prolongado en cama tenía consecuencias perjudiciales en el tratamiento de la enfermedad, y que la actividad física debería estar limitada solamente a prevenir los síntomas.
Un estudio clásico de Levine y Lown (1952) incluyó 81 pacientes con IM agudo que estaban sujetos a "tratamiento de sillón" y a los que se les liberó de la restricción de actividad apenas después de un evento coronario agudo. La mayoría de los pacientes salían de la cama y se sentaban en una silla hasta 2 horas durante el primer día de hospitalización. La duración en la silla se incrementaba progresivamente durante el tiempo en el hospital, y se les incentivaba a comer por sus propios medios y usar chatas al lado de la cama o el baño. Casi todos fueron dados de alta luego de 4 semanas. No hubo complicaciones atribuidas a la intervención, y la tasa de mortalidad de pacientes tratados con el reposo en el sillón fue menor que la del grupo control que había recibido terapia convencional (reposo en cama). Estos resultados han sido respaldados ahora por numerosos estudios clínicos controlados (Grines y cols., 1993), mostrando evidencias convincentes de que la movilización temprana y el alta hospitalaria precoz de pacientes con IM no complicado es una práctica segura que está asociada a numerosos beneficios fisiológicos, psicológicos y económicos. Actualmente, muchos pacientes post-IM son dados de alta del hospital a los 3-6 días.
Los estudios recientes sugieren que la falta de estrés ortostático es más importante que la inactividad física en cuanto a la producción de los efectos perjudiciales del reposo en cama; por consiguiente, las intervenciones para simular el estrés gravitacional son ampliamente utilizadas para prevenir o atenuar estas consecuencias. Convertino y cols. (1982) estudiaron los cambios en el VO2 máx., antes y después de 14 días de reposo en cama utilizando tratamientos diarios con un traje de inclinación reversa que simulaba los efectos de estar parado. La capacidad aeróbica disminuyó sólo un 6% en los sujetos que recibieron tratamientos de mejoría del retorno venoso, en comparación con el 15% en los sujetos control no tratados (Tabla 2). Estos datos tienen implicancias importantes para la rehabilitación cardiaca hospitalaria. La pérdida de estrés gravitacional sola, durante el reposo en cama en la fase hospitalaria, contribuye a la disminución del VO2 máx. luego de un IM, independientemente de las variables clínicas relacionadas (por ej., fracción de eyección). Por lo tanto, aparentemente la simple exposición a un estrés ortostático o gravitacional, como sentarse o pararse en forma intermitente durante el período de internación, podría obviar gran parte del deterioro en el rendimiento físico que normalmente sigue a un evento coronario agudo (Convertino, 1983). La tera-pia física formalizada en el hospital luego de un IM agudo parece ofrecer pocos beneficios fisiológicos o de comportamiento (autoeficacia) adicionales al cuidado médico de rutina (Sivarajan y cols., 1981; Oldridge y Rogowski, 1990).

Tabla 2. Cambios medios en el máximo consumo de Oxígeno (VO2
máx), antes y después del reposo en cama (*)
(*) Adaptado de Convertino y cols., 1982.
CANTIDAD NECESARIA DE EJERCICIO PARA EL PACIENTE CON ENFERMEDAD EN LAS ARTERIAS CORONARIAS
Se ha mostrado que niveles más bajos de actividad física que los previamente recomendados reducen el riesgo de ciertas enfermedades crónicas degenerativas pero aún son insuficientes para mejorar el VO2 máx. El ejercicio a intensidades moderadas (≤ al 60% del VO2 máx) puede producir numerosos beneficios para la salud, incluyendo mejorías en el bienestar psico-social, en la densidad ósea, tolerancia a la glucosa y en los factores de riesgo coronario, así como una reducción en la mortalidad relacionada con causas cardiovasculares. Además, aparentemente el entrenamiento físico de baja y alta intensidad produce incrementos comparables en la capacidad funcional y en el colesterol con lipoproteínas de alta densidad (HDL) en pacientes cardiacos desentrenados, al menos durante los 3 a 12 meses iniciales de acondicionamiento (Blumenthal y cols., 1988; Goble y cols., 1991). La Figura 3 muestra la relación teórica entre los beneficios sobre la salud y la capacidad cardiorrespiratoria, estimados a partir de aumentarlas dosis de ejercicios. Aparentemente, los beneficios sobre la salud pueden ocurrir con niveles o intensidades más bajas, es decir con cantidades que podrían no necesariamente mejorar la capacidad aeróbica. Sin embargo, tales programas normalmente están asociados con una mayor duración de ejercicio, mayor frecuencia, o ambas.
Dentro de las 3 a 11 semanas luego de IM, CABGS, o PTCA clínicamente sin complicaciones, generalmente se produce un incremento "espontáneo" en la capacidad aeróbica o VO2 máx. limitado por la fatiga, aún en pacientes que no realizan un entrenamiento físico normal (Savin y cols., 1981; Weiner y cols., 1981; Ben-Ari y cols., 1989). Esto se debe supuestamente a que el cuidado personal y otras actividades fuera del hospital, llevadas acabo por los pacientes cardíacos apenas después de abandonar el mismo, llevan a incrementar de manera sostenida el consumo de oxígeno que puede superar la intensidad "umbral", la cual para la mayoría de pacientes desentrenados con enfermedades en las arterias coronarias podría rondar entre el 40% y el 60% del VO2 máx. (Sheldahl y cols., 1984; Franklin y cols., 1992). No obstante, la capacidad aeróbica puede aumentarse aún más a través de programas de acondicionamiento físico en el gimnasio o en el hogar (DeBusk y cols., 1979).
Los incrementos en el VO2 máx entre pacientes cardiacos varía entre el 11 y el 66% luego de 3 a 6 meses de entrenamiento físico, con los mayores aumentos entre los más desentrenados (Balady y cols., 1994). El beneficio más consistente parece ocurrir con un entrenamiento de al menos 3 veces por semana durante 12 semanas o más, 20-40 minutos por sesión, a una intensidad aproximada al 70-85% de la frecuencia cardiaca máxima (Wenger y cols., 1995). Sin embargo, intensidades de 50-70% en el rango de frecuencia cardiaca, correspondientes al 40-60% del VO2 máx., han mostrado tener un efecto similar sobre la mejoría en la capacidad funcional en pacientes desacondicionados (Blumenthal y cols.,1988). La intensidad umbral parece aumentar en proporción directa con el VO2 máx. pre-entrenamiento (Figura 4). El aumento en la capacidad aeróbica con intensidades bajas a moderadas sugiere que la interrelación entre intensidad de entrenamiento, frecuencia, y duración podría permitir una disminución en la intensidad, que es parcial o totalmente compensada por los aumentos en la duración del ejercicio o en la frecuencia, o ambos.
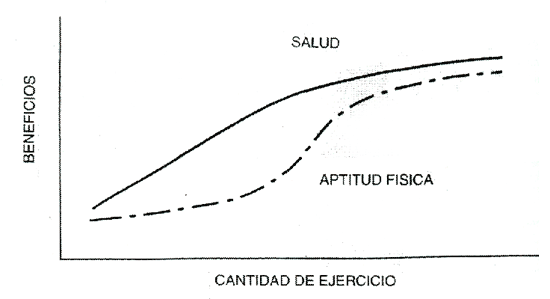
Figura 3. Relación teórica entre beneficios sobre la salud y la aptitud
física ("fitness"), y la cantidad o intensidad de ejercicio.
A pesar de que se cree que los beneficios aeróbicos del ejercicio se consiguen sólo con sesiones continuas de 30 minutos o más, algunos estudios recientes han mostrado mejorías en la capacidad cardiorresiratoria en sujetos que completaron tres series de 10 minutos de intensidad moderada por día, en comparación con aquellos que realizaban una serie continua de 30 minutos, 5 veces por semana, durante 8 semanas (DeBusk y cols., 1990). El aumento relativo en el VO2 máx. fue significativamente mayor en el grupo con la serie continua (13.9% vs. 7.6%); sin embargo, ambos grupos mostraron idénticos porcentajes de incremento y disminución en la duración en el test de esfuerzo y en la frecuencia cardiaca submáxima, respectivamente (Table 3). De manera similar, un grupo de sujetos que fue aleatoriamente asignado a uno de tres grupos que corrieron la misma distancia total, pero en una, dos, o tres sesiones diarias, mostraron mejorías comparables en la capacidad cardiorrespiratoria (medida mediante VO2 máx.); sin embargo, los niveles de lipoproteínas de alta densidad en el colesterol incrementaron significativamente sólo en el grupo que entrenaba tres veces por día (Ebisu, 1985). Por lo tanto, los incrementos relativos en la capacidad funcional parecen depender más del "fitness" o aptitud física inicial del sujeto y de la cantidad total de ejercicio realizado o de las kilocalorías (kcal) gastadas, que de la frecuencia, intensidad, o duración específicas del ejercicio.
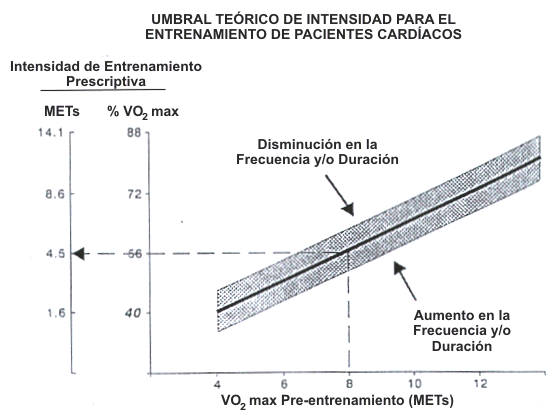
Figura 4. Relación teórica entre capacidad aeróbica (expresada como
equivalentes metabólicos; METs) y la intensidad mínima para el entrenamiento
físico, expresada como porcentaje del máximo consumo de Oxígeno (VO2
máx.). La intensidad umbral del entrenamiento aumenta en proporción directa
con el VO2 máx. antes del mismo; sin embargo, puede modularse
alterando la duración o frecuencia del ejercicio, o ambas. Por ejemplo, un
paciente con una capacidad pico de 8 METs estaría entrenando a aproximadamente
el 56% de su VO2 máx.,o 4.5 ±0.5 METs, para incrementar más su
capacidad funcional.
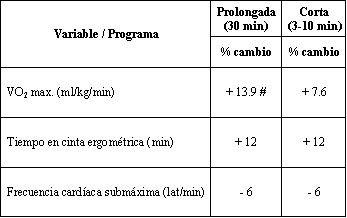
Tabla 3. Efectos del entrenamiento con series de ejercicio prolongadas vs.
cortas, en sujetos sanos (*)
(*)Adaptado de DeBusk RF y cols., 1990.
(#) p = 0.03 vs. series cortas.
Entrenamiento de resistencia muscular con la parte superior del cuerpo
Es nuevo de esta década la demostración de que el ejercicio aeróbico con la parte superior del cuerpo, y el entrenamiento suave a moderado de la resistencia, pueden mejorar segura y efectivamente la fuerza y la resistencia muscular en pacientes coronarios clínicamente estables. Además, los estudios recientes con pacientes post-IM sugieren que los brazos responden al entrenamiento aeróbico de manera cuantitativa y cualitativamente similar que las piernas (Franklin y cols., 1994). Los programas anexos con el tronco superior y con ejercicios de resistencia facilitan, además, una mayor transferencia de los beneficios del entrenamiento a las actividades laborales y recreacionales, y brindan mayor diversidad al régimen de acondicionamiento, lo cual podría aumentar la adherencia y el interés de los pacientes.
Las adaptaciones cardiorrespiratorias y metabólicas al ejercicio parecen ser bastante específicas a los grupos musculares que han sido entrenados (Figura 5) (Clausen y cols., 1970). Por lo tanto, por primera vez, el principio de especificidad del entrenamiento, tan reconocido como guía importante para el entrenamiento de los deportistas, ha sido incorporado a la rehabilitación cardiaca para incentivar el retorno a las tareas laborales específicas y a las actividades recreativas. La poca capacidad de intercambio en los beneficios del entrenamiento entre unas extremidades y otras parece desacreditar la práctica general para prescribir ejercicios sólo para piernas (Franklin, 1985). En consecuencia, los pacientes cardíacos que realizan actividades con las extremidades superiores deberían entrenar los brazos así como las piernas, con la expectativa de atenuar las respuestas cardiorrespiratorias y hemodinámicas de ambas formas de esfuerzo.
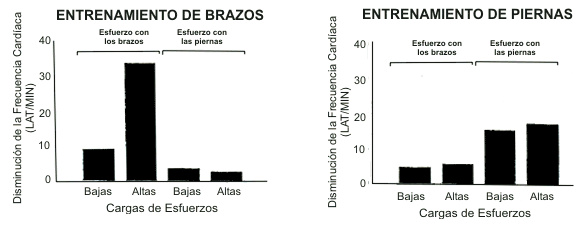
Figura 5. A. El entrenamiento de brazos utilizando cicloergómetro
disminuyó marcadamente la respuesta de la frecuencia cardiaca durante
ejercicios de brazos con cargas bajas y altas, mientras que la reducción de la
frecuencia cardiaca durante un esfuerzo con las piernas fue menor. B. De
manera similar, el entrenamiento de piernas disminuyó notoriamente la
frecuencia cardiaca durante los esfuerzos con las piernas, mientras que la
reducción fue mínima con esfuerzos de brazos. Adaptado de Clausen y cols.,
1970.
La razón para apoyar el entrenamiento de la resistencia como complemento de la rehabilitación cardiaca proviene de varias líneas de evidencia. Debido a que la magnitud de la respuesta presora al esfuerzo estático es proporcional al porcentaje de contracción voluntaria máxima (CVM)(Lind y McNichol, 1967), así como a la masa muscular involucrada (Mitchell y cols., 1980), cualquier incremento en la fuerza debería resultar en un menor producto tasa-presión a una carga determinada debido a que la misma ahora representa un menor porcentaje de CVM (Lewis y cols., 1984). También hay datos interesantes que sugieren que el entrenamiento de la resistencia puede aumentar el tiempo de "endurance" hasta el agotamiento tanto en cinta como en bicicleta ergométrica sin un incremento paralelo en el VO2 máx. (Hickson y cols., 1980). Además, el entrenamiento progresivo de resistencia podría tener un efecto favorable sobre la presión sanguínea en reposo y sobre los niveles de lípidos y lipoproteínas (Goldberg y cols., 1984).
En las Tablas 4 (Franklin, 1985) y 5 (Feigenbaum y Pollock, 1997) se muestran los lineamientos modernos para el ejercicio dinámico con el tronco superior (ergómetro de brazos) y el entrenamiento de resistencia, respectivamente.

Tabla 4. Lineamientos para el entrenamiento dinámico con los brazos (*).
(*)Adaptado de Franklin, 1985.
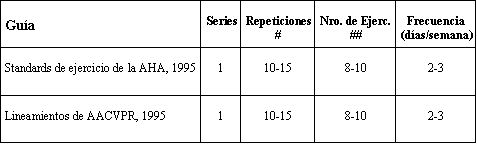
Tabla 5. Lineamientos para el entrenamiento de la resistencia con
pacientes cardíacos (*).
AHA =Asociación Americana del Corazón; AACVPR=Asociación Americana de
Rehabilitación Cardiovascular y Pulmonar. (*) Adaptado de Feigenbaum y Pollock,
1997. (#) Para pacientes cardíacos, el peso debería ser suficiente para
inducir fatiga muscular con el número de repeticiones estipuladas. No
obstante, se podrían emplear cargas más livianas. (##) Mínimo un ejercicio por
grupo muscular principal.
Detención y reversión de las enfermedades cardiacas
Para determinar la cantidad de actividad física (kcal/sem) necesaria para retardar la progresión de lesiones ateroescleróticas coronarias, Hambrecht y cols. (1993) estudiaron los efectos del entrenamiento físico y una dieta con bajo contenido de grasa, sin agentes concomitantes de disminución de lípidos, sobre la morfología coronaria en pacientes con angiografía coronaria basal y angina de pecho estable. El grupo experimental con ejercicio-dieta (n = 29) fue comparado con un grupo control (n = 33) que recibió los cuidados usuales. En el grupo experimental se observó regresión de enfermedades coronarias, o ningún cambio, en la morfología coronaria en 26 pacientes (90%), en comparación con 18 pacientes (55%) en el grupo control. Los mayores niveles de actividad física recreativa estuvieron asociados ya sea con ningún cambio, o con la reversión de lesiones ateroescleróticas coronarias (Figura 6). Estos resultados sugieren que un mínimo de 1600 kcal/sem de actividad física podría detener la progresión de enfermedades coronarias, mientras que un gasto calórico de 2200 kcal/sem podría lograr la regresión. Para muchos pacientes, estas metas requerirían caminar 24 y 32 km (15 y 20 millas) por semana, respectivamente.
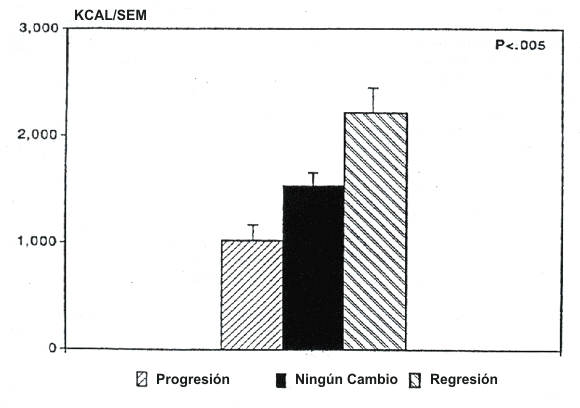
Figura 6. Efectos de la actividad física sobre la morfología coronaria en
los grupos experimental y control combinados. Los niveles más bajos de
actividad se observaron en pacientes con progresión de enfermedad en las
arterias coronarias (1022 ±142 kcal/sem),en comparación con paciente sin
cambio (1533 ±122 kcal/sem) (p < 0.005). Adaptado de Hambrecht y cols., 1993.
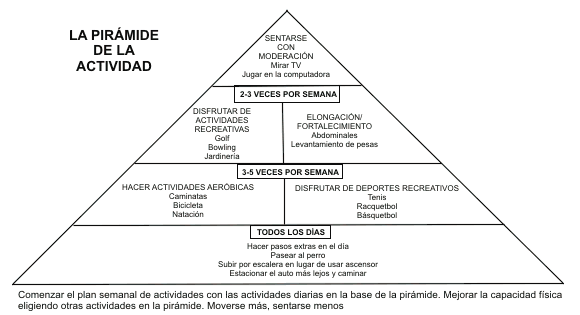
Figura 7. La Pirámide de Actividad, análoga a la Pirámide de Alimentos de
USDA, ha sido sugerida como modelo para facilitar la educación del publico en
general y del paciente para adoptar un estilo de vida progresivamente más
activo. Copyright 1996, Park Nicollet Healthsource. Instituto para la
Investigación y la Educación. Reimpreso con permiso.
En resumen, en un informe consensuado sobre la prevención de ataques cardíacos y muerte en pacientes con enfermedades coronarias se subrayó la importancia de realizar un mínimo de 30 a 60 minutos de actividad moderada, 3 a 4 veces por semana, complementada con un aumento en las actividades de la vida cotidiana (por ej., pausas en el trabajo para caminar, usar escaleras, hacer trabajos de jardinería, trabajos en la casa, etc.); se sugirieron de 5 a 6 horas por semana para lograr los mayores beneficios cardioprotectores (Smith y col s.,1995). Con respecto a esto, puede ser útil incrementar la actividad física de la vida diaria (Figura 7) (Leon y Norstrom, 1995).
SEGURIDAD DE LA REHABILITACIÓN CARDIACA BASADA EN EL EJERCICIO
A pesar de que la incidencia de complicaciones cardiovasculares durante el ejercicio es considerablemente mayor entre pacientes cardíacos que entre adultos presumiblemente sanos, aún así es relativamente baja. De acuerdo a un estudio ampliamente publicado, la incidencia de complicaciones fue de un paro cardíaco por 111.996 horas-paciente, un IM por 293.990 horas-paciente, y un caso fatal por 783.972 horas-paciente de rehabilitación cardíaca (Van Camp y Peterson, 1986). Sin embargo, se debería enfatizar que esta tasa de mortalidad aparentemente baja se aplica solamente a programas médicamente supervisados, equipados con defibrilador y adecuadas drogas de emergencia. Los informes recientes indican que hasta el 90% de todos los pacientes con paro cardíaco, que ocurren bajo tales condiciones, son exitosamente reanimados.
Variables que afectan la seguridad del paciente
La seguridad del paciente durante los programas de entrenamiento podría mejorarse a través de una cuidadosa evaluación médica preliminar y atención a los procesos de acondicionamiento físico y monitoreo. Aparentemente, el monitoreo continuo del ECG en pacientes seleccionados con riesgo moderado a alto durante la sesión de ejercicio y/o la supervisión médica más de cerca (por ej. una relación paciente/ staff médico más baja) podría resultar en una mayor seguridad al paciente, identificando los signos o síntomas sugerentes de un mayor riesgo. Además, la supervisión de cerca ayuda evitar que los pacientes superen las intensidades estipuladas y reduce la posibilidad de provocar isquemia miocárdica o inestabilidad eléctrica, ya que estas podrían ser precursoras de fibrilación ventricular. Otros factores que podrían aumentar la seguridad del paciente incluyen la incentivación a controlarse el pulso (a través de método palpatorio o con cardiotacómetros), la disponibilidad de supervisión médica con apropiado equipamiento para emergencias, uso de defibriladores, registrar los ritmos del ECG en reposo y en ejercicio (Franklin y cols., 1989), la administración de drogas antiarrítmicas para los pacientes con serias arritmias ventriculares, ejecución estricta de las frecuencias cardíacas prescriptas para mantener intensidades suaves a moderadas, adherencia a procedimientos adecuados de entrada en calor y vuelta a la calma (Haskell, 1978), y atención al mantenimiento de los niveles de potasio en suero.
El concepto de frecuencia cardiaca a alcanzar ("target") (TFC) tiene varias ventajas importantes para controlar la intensidad del ejercicio. Por ejemplo, una TFC (por ej., 120 lat/min) que se establece durante el acondicionamiento físico, puede ser aplicada fuera del gimnasio en las actividades laborales o de tiempo libre. La TFC tiene un regulador incorporado para los cambios en el fitness, permitiendo por lo tanto al paciente mantener la misma intensidad relativa a lo largo de un programa de ejercicio. A medida de que el paciente va teniendo una mejor condición física, la velocidad de la caminata o la resistencia en la bicicleta ergométrica debe ser lentamente incrementada para compensarla disminución en la frecuencia cardiaca producida por el acondicionamiento. Por lo tanto, la TFC alcanzada inicialmente con un nivel dado de esfuerzo, en el futuro sólo puede lograrse con un esfuerzo mayor. Las frecuencias cardíacas prescriptas también brindan los extremos en condiciones ambientales. Por ejemplo, en climas calurosos o húmedos se requiere menos trabajo para alcanzar una TFC específica (Pandolf y cols., 1975), aún a pesar de que el esfuerzo del corazón (consumo de Oxígeno miocárdico) permanece sin cambiar. El sujeto que está entrenado para controlarse la TFC también es capaz de detectar arritmias y sabrá disminuir el ritmo de entrenamiento y/o buscar ayuda médica.
ASPECTOS VOCACIONALES U OCUPACIONALES
Desafortunadamente, la ayuda ocupacional, a menudo, no se enfatiza lo suficiente en los programas contemporáneos de rehabilitación cardiaca. Sin embargo, una evaluación de las tareas laborales en pacientes cardíacos jóvenes y de mediana edad podría acelerar el retorno al trabajo porque les asegura a ellos y a sus médicos de cabecera que el estrés físico, psicológico, y ambiental asociado con la profesión puede ser tolerado de manera segura. Para tales pacientes un pronto retorno al trabajo también podría resultar en un significativo ahorro en los costos. Dennis y cols. (1988) demostraron que los pacientes empleados, con IM clínicamente sin complicaciones, que se sometieron una evaluación de tareas laborales (test en cinta limitado por los síntomas y ayuda con consejero) 23±3 días después de su evento coronario agudo volvieron al trabajo antes que los pacientes que recibieron el cuidado normal, 51 y 75 días, respectivamente. Este retorno más precoz al trabajo estuvo asociado con $ 2.102 de salario adicional ganado por el paciente experimental, en los seis meses luego del IM, a pesar de la tasa comparable de eventos cardíacos recurrentes, en comparación con el grupo control.
Debido a que la automatización y mecanización han eliminado muchos trabajos que requieren esfuerzos físicos intensos, la capacidad funcional a disminuido marcadamente como determinante de la capacidad de ser empleado luego de un evento coronario agudo. En el mercado laboral actual, el nivel de riesgo coronario es mucho más importante que la capacidad funcional para determinar el potencial para el trabajo (DeBusk, 1992). Además, las condiciones económicas nacionales y locales, numerosas variables no médicas, consideraciones psicológicas, estereotipos de los empleadores, y la disponibilidad de los beneficios de la pensión, parecen tener mayor influencia sobre los porcentajes del retorno al trabajo que la capacidad aeróbica.
TERAPIAS ABARCATIVAS DE REDUCCIÓN DE RIESGOS
Hasta la mitad de la década del '80, la prevención secundaria de la ateroesclerosis apuntaba principalmente a la ambulación temprana, entrenamiento físico, y a una dieta "prudente". Estos regímenes generalmente resultaban en una mejor capacidad funcional, menor demandas miocárdica a intensidades submáximas, y disminuciones modestas en la mortalidad cardiovascular. Sin embargo, las tasas de reinfarto y el curso de la enfermedad cardiaca ateroesclerótica permanecían sin cambios. Ahora los estudios contemporáneos sugieren que la modificación multifactorial de los factores de riesgo, y especialmente las variables más intensivas para controlar la hiperlipidemia con la dieta, drogas, y ejercicio (Tabla 6) (Tran y Brammell, 1989), podrían retardar, detener, y aún revertir la progresión de enfermedades ateroescleróticas en las arterias coronarias. Entre otros beneficios se incluyen la reducción de síntomas anginosos, disminuciones en la isquemia miocárdica inducida por el ejercicio, menores eventos cardíacos recurrentes, y una menor necesidad de realizar PTCA o CABGS. Varios mecanismos podrían contribuir a estas mejorías en los resultados clínicos, incluyendo la estabilización plaquetaria, la regresión anatómica parcial (aunque pequeña) de la estenosis de las arterias coronarias, una menor incidencia de ruptura de placas, y una mejor función del endotelio coronario. Estos resultados sugieren un nuevo paradigma en el tratamiento de pacientes con enfermedades en las arterias coronarias (Franklin y Kahn, 1996).
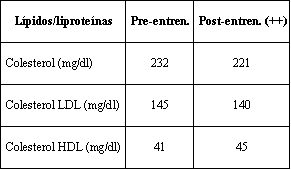
Tabla 6. Efectos del entrenamiento físico (*) sobre los niveles de lípidos
en suero en pacientes post-infarto de miocardio: un meta-análisis (+).
(*) La intensidad promedio de ejercicio fue del 74 + 7% de la frecuencia
cardiaca máxima.
(+) Adaptado de Tran y Brammell, 1989.
(++) Todos los valores fueron significativamente diferentes de los valores de
pre-entrenamiento
LDL = lipoproteína de baja densidad; HDL = lipoproteína de alta densidad
Recientemente, Superko y Krauss (1994) revisaron en forma crítica 10 estudios clínicos randomizados (muestras al azar) y controlados que utilizaron arteriografía coronaria para evaluar el efecto de la manipulación de las lipoproteínas sobre la tasa de progresión y regresión de lesiones ateroescleróticas coronarias en un total de 2.095 participantes. Tres estudios usaron un método no farmacológico (por ej., dieta y/o ejercicio), y 7 usaron terapia medicamentosa simple o múltiple combinada con dieta. El grupo farmacológico tuvo una reducción 17% mayor de triglicéridos, 8% mayor de colesterol total, 13% mayor de lipoproteínas de baja densidad (LDL), y un aumento 14% mayor en las lipoproteínas de alta densidad (HDL), en comparación con el grupo no farmacológico. La comparación general de los resultados arteriográficos en los grupos experimental y control reveló 24% más de progresión en el grupo control (53% vs. 29%) y 20% más de progresión en los grupos experimentales (31 % vs. 11 %) (Figura 8). Los eventos clínicos fueron menores en los grupos experimentales; en algunos estudios esto alcanzó significancia estadística. En conjunto, estos trabajos indican que la manipulación agresiva de las lipoproteínas puede reducir significativamente la progresión de las enfermedades en las arterias coronarias, promover la regresión, y reducir los eventos clínicos en un tiempo relativamente breve de tratamiento entre 2 y 4 años.
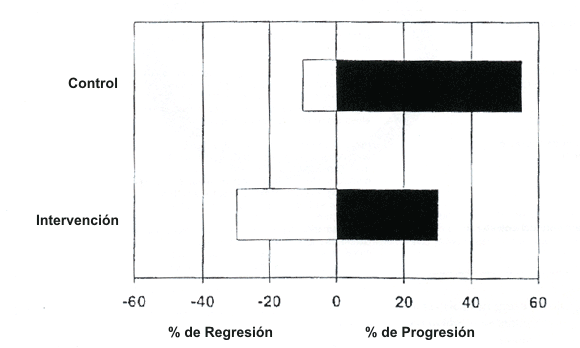
Figura 8. Porcentaje promedio de pacientes que revelan evidencia
arteriográfica de regresión y progresión, en 10 estudios con grupos control,
que fueron tenidos en cuenta para la comparación. Los grupos control se
muestran arriba y los grupos experimentales abajo. Adaptado de Superko y
Krauss, 1994.
A pesar de que el potencial para la regresión de la ateroesclerosis coronaria ha sido preconizado por algunos como el principal mecanismo responsable de la mejoría en los resultados clínicos, el cúmulo de evidencia sugiere que la estabilidad plaquetaria es aún más importante que la regresión. Estudios recientes han mostrado que el IM agudo en pacientes médicamente tratados con enfermedades en las arterias coronarias ocurre frecuentemente en sitios con > 70% de obstrucción en un angiograma anterior (Little y cols., 1988; Little y cols., 1990). Esto podría explicar además porqué ha sido difícil observar una reducción en la incidencia de IM no fatales en la mayoría de los estudios que examinan los efectos de la revascularización coronaria. Además, es interesante compararlas alteraciones en la obstrucción del lumen que ocurrieron en respuesta al tratamiento agresivo sobre las lipoproteínas en los estudios de regresión (1 a 7%), con la reducción en los eventos clínicos (22 a 79%). Esto sugiere que la estabilidad plaquetaria (más que la regresión) está más estrechamente relacionada con la reducción de eventos clínicos. Cada paciente con enfermedad en las arterias coronarias tiene numerosas plaquetas y la mayoría no mejora a pesar del tratamiento agresivo sobre las lipoproteínas. Las lesiones que tienden a provocar eventos coronarios agudos no son las que están obstruidas en un 90% sino aquellas con una estenosis del 50 al 75%, las que previamente se pensaba que eran benignas. La inestabilidad plaquetaria que resulta en estos eventos podría mejorarse dramáticamente a través de las reducciones en el colesterol en sangre, a pesar de no producirse cambios en el estrechamiento de la arteria coronaria (Smith, 1996).
Recientemente, un panel de expertos de la Asociación Americana del Corazón publicó una serie de estrategias de reducción de riesgos diseñadas para prolongar la expectativa general de vida, mejorar la calidad de la misma, disminuir la necesidad de revascularización, y reducir, por consiguiente, los eventos cardiovasculares en pacientes con enfermedades vasculares y en las arterias coronarias (Smith y cols., 1995). Estas estrategias consensuadas fueron aprobadas por el Colegio Americano de Cardiología, y ampliadas para incluir las intervenciones con homocisteína (vitaminas B), y la ayuda psico-social; las mismas pueden ser resumidas como el ABCDE de la prevención secundaria (Tabla 7).
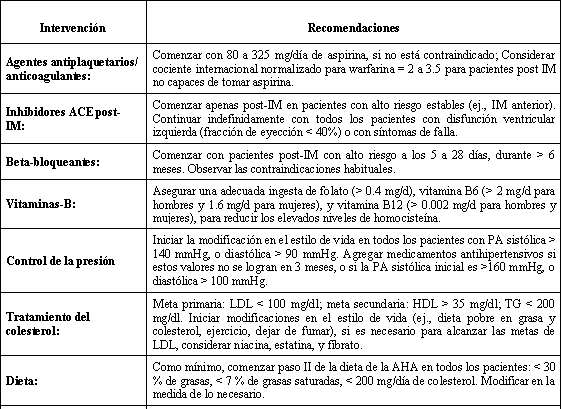

Tabla 7. ABCDE de la prevención secundaria: Estrategias abarcativas de
reducción de riesgo para pacientes con enfermedades coronarias y otras
enfermedades vasculares (*).
IM = infarto de miocardio; PA = presión arterial; LDL = lipoproteínas de baja
densidad; HDL = lipoproteínas de alta densidad; TG = triglicéridos; AHA =
Asociación Americana del Corazón. (*) Adaptado de Smith y cols., 1995.
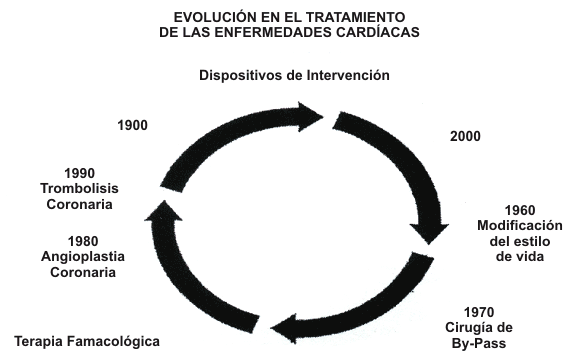
Figura 9. En los años ’60 el tratamiento de la enfermedad cardiaca
comprendía, en gran parte, la modificación del estilo de vida. Desde entonces,
han surgido la cirugía, la farmacoterapia intensiva, y las técnicas
intervencionistas. Sin embargo, estudios recientes han mostrado que la
reducción agresiva de los factores de riesgo, incluyendo el entrenamiento
físico, pueden estabilizar, y aun revertir, el proceso ateroesclerótico.
CONCLUSIONES
Los avances tecnológicos en el diagnóstico, imagen, y terapias médicas, y los procedimientos intervencionistas, incluyendo el cardiovertor desfibrilador implantable, han mejorado notablemente en cuidado de la enfermedad cardiaca y han reducido el riesgo de muerte súbita cardiaca. El tratamiento ha evolucionado desde la simple modificación del estilo de vida en la mitad de la década del 60, hasta un amplio rango de costosas intervenciones médicas y quirúrgicas (Figura 9) que a menudo no pueden dirigirse a las causas subyacentes - dietas ricas en grasa y colesterol, tabaquismo, hipertensión, y sedentarismo.
En la puerta del segundo milenio, aún sigue estando la necesidad de que los profesionales de la salud implementen terapias amplias de educción de riesgos para pacientes con enfermedades cardiovasculares, y aumentar la adherencia de los pacientes a las mismas (Franklin y cols., 1997). Este enfoque costo-efectividad, el cual es ahora fuertemente respaldado por la investigación científica, es bastante promisorio. El desafío es convertir esta promesa en realidad.
Referencias
1. Asher, R.A.J (1947). Dangers of going to bed. British Medical Journal, 2, 967-968
2. Balady, G.J., Fletcher, B.J., Froelicher, E.S., Hartley, L.H., Krauss, R.M., Oberman, A., Pollock, M.L. and Taylor, C.B (1994). Cardiac rehabilitation programs. A statement for healthcare professionals from the American Heart Association. Circulation, 90,1602-1610
3. Ben-Ari, E., Rothbaum, D.A., Linnerneir, T.J., Landin, R.J., Steinmetz., E.F., Hillis, SJ., Noble, J.R., Hallam, C.C., See, M.R. and Shiner, R (1989). Benefits of a monitored rehabilitation program versus physician care after emergency percutaneous transluminal coronary angioplasty: follow-up of risk factors and rate of restenosis. Journal of Cardiopulmonary Rehabilitation, 9, 281-285
4. Blumenthal, J.A., Rejewski, W.J., Walsh-Riddle, M., Emery, C.F., Miller, H., Roark, S., Ribisl, P.M., Morris, P.B., Brubaker, P. and Williams, R.S (1988). Comparison of high- and low-intensity exercise training early after acute myocardial infarction. American Journal of Cardiology, 61, 2630
5. Boushey, C.J., Beresford, S.A.A., Omenn, G.S. and Motulsky, A.G (1995). A quantitative assessment of plasma homocysteine as a risk factor for vascular disease. Probable benefits of increasing folic acid intakes, Journal of the American Medical Association, 274, 1049-1057
6. Clausen, J.P., Trap-Jcnsen, J. and Lasscn, N.A (1970). The effects of training on the heart rate during arm and leg exercise. Scandinavian Journal of Clinical and Laboratory -Investigation
7. Convertino, V.A (1983). Effects of orthostatic stress on exercise performance after bed rest; relation to inhospital rehabilitation. Journal of Cardiac Rehabilitation. 3, 660-663
8. Convertino, V.A., Sandler, H., Webb, P. and Annis, J.R (1982). Induced venous pooling and cardiorespiratory responses to exercise after bedrest. Journal of Applied Physiology, 52, 1343-1348
9. DeBusk, R.F (1992). Why is cardiac rehabilitation not widely used?. Western Journal of Medicine, 156, 206-208
10. DeBusk, R.F, Houston, N., Haskell, W., Fry, G. and Parker, M (1979). Exercise training soon after myocardial infarction. American Journal o Cardiology, 44, 1223-1229
11. DeBusk, R.F., Blomgvist, C.G., Kouchoukos, N.T., Luepker, R.V., Miller, H.S., Moss, A.J., Pollock, M.L., Reeves, T.J., Selvester, R.H. and Stason, W.B (1986). Identification and treatment of lowrisk patients after acute myocardial infarction and coronary-artery bypass graft surgery. New England Journal of Medicine, 314, 161-166
12. DeBusk, R.F., Stenestrand, U., Sheehan, M. and Haskell, W.L (1990). Training effects of long versus short bouts of exercise in healthy sub-jeets. American Journal of Cardiology, 65, 1010-1013
13. Dennis, C., Houston-Miller, N., Schwartz, R.G., Alin, D.K., Kraemer, H.C., Gossard, D., Juneau, M., Taylor, C.B. and DeBusk, R.F (1988). Early return to work after uncomplicated myocardial infarction. Results of a randomized trial. Journal qf the American Medical Association, 260, 214 - 220
14. Ebisu, T (1985). Splitting the distance of endurance running: on cardiovascular endurance and blood lipids. Japanese Journal of Physical Education, 30. 37-43
15. Feigenbawn, M.S. and Pollock, M.L (1997). Strength training: Rationale for current guidelines for adult fitness programs. The Physician and Sportsmedicine, 25, 44-64
16. Franklin, B.A (1985). Exercise testing, training and arm ergometry. Sports Medicine, 2, 100-119
17. Franklin, B.A (1991). Introduction: physiologic adaptations to exercise training in cardiac patients: contemporary issues and concerns. Medicine and Science irr Sports and Exercise, 23, 645-647
18. Franklin, B.A. and Kahn, J.K (1996). Delayed progression or regression of coronary atherosclerosis with intensive risk factor modification... Effects of diet, drugs, and exercise. Sports Medicine, 22, 306-320
19. Franklin, B.A., Reed, PS., Gordon, S. and Timmis, G.C (1989). lnstantaneous electrocardiography. A simple screening technique for cardiac exercise programs. Chest, 96, 174-177
20. Franklin, B.A., Gordon, S. and Timmis, G.C (1992). Amount of exercise necessary for the patient with coronary artery disease. American Journal of Cardiology, 69, 1426-1432
21. Franklin, B.A., Vander, L., Wrisley, D. and Rubenfire, M (1994). Trainability of arias versus legsin men with previous myocardial infarction. Chest. 105, 262-264
22. Franklin, B.A., Hall, L. and Timmis, G.C (1997). Contemporary cardiac rehabilitation services. American Journal of Cardiology, 79, 1075-1077
23. Friedberg, C.K (1966). Diseases of the Heart (3rd ed). Philadelphia, PA: WB Saunders
24. Goble, A.J., Hare, D.L., Macdonald, P.S., Oliver, R.G., Reid, M.A. and Worcester, M.C (1991). Effect of early programmes of high and low intensity exercise on physical performance after transmural acute myocardial infarction. British Heart Journal, 65, 126-13 1
25. Goldberg, L., Elliot, D.L., Schutz, R.W. and Kloster, F.E (1984). Changes in lipid and lipoprotein levels after weight training. Journal of the American Medical Association, 252, 5 04-5 06
26. Gould, L.K., Ornish, D., Sherwitz, L., Brown, S., Edens. R.P, Hess, M.J., Mullani, N., Bolomey, L., Dobbs, F. and Armstrong, W.T (1995). Changes in myocardial perfusion abnormalities by positron emission tomography after long-term, intense risk factor modification. Journal of the Arnerican Medical Association, 274. 894-901
27. Grines, C.L., Browne, K.F, Marco, J., Rothbaum, D., Stone, G.W., O'Keefe, J., Overlie, P. Donohue, B., Chelliah, N. and Timmis, G.C for the Primary Angioplasty in Myocardial Infarction Study Group (1993). A comparison of immediate angioplasty with thrombolytic therapy for acute myocardial infarction. New England Journal o Medicine, 323, 673-679
28. Hambrecht, R., Niebauer, J., Marburger, C., Grunze, M., Kdlberer, B., Hauer, K., Schlierf, G., Ktibler, W. and Schuler, G (1993). Various intensities of leisure time physical activity in patients with coronary artery disease: effects on cardiorespiratory fitness and progression of coronary atherosclerotic lesions. Journal of the American College of Cardiology, 22, 468-477
29. Harrison, T.R (1944). Abuse of rest as a therapeutic measure for patients with cardiovascular disease. Journal of the American Medical Association, 125, 1075-1077
30. Haskell, W.L (1978). Cardiovascular complications during exercise training of cardiac patients. Circulation, 57, 920-924
31. Haskell, W.L., Alderman, E.L., Fair, J.M., Maron, D.J., Mackey, S.F., Superko, H.R., Williams, P.T., Johnstone, I.M., Champagne, M.A. and Krauss, R.M (1994). Effects of intensive multiple risk factor reduction on coronary atherosclerosis and clinical cardiac events in men and women with coronary artery disease. The Stanford Coronary Risk Intervention Project (SCRIP). Circulation, 89, 975-990
32. Hickson, R.C., Rosenkoetter, M.A. and Brown, M.M (1980). Strength training effects on aerobic power and short-term endurance. Medicine and Science in Sports and Exercise, 12, 336-339
33. Lau, J., Antman, E.M., Jimenez-Silva, J., Kupelnick, B., Mosteller, F. and Chalmers, T. C (1992). Cumulative meta-analysis of therapeutic trials for myocardial infarction. New England Journal of Medicine, 327, 248-254
34. Leon, A.S. and Norstrom, J (1995). Evidence of the role of physical activity and cardiorespiratory fitness in the prevention of coronary heart disease. Quest, 47, 311-319
35. Levine, S.A. and Lown, B (1952). Armchair treatment of acute coronary thrombosis. Journal of the American Medical Association, 148, 1365-1369
36. Lewis, S., Nygaard, E., Sanchez, J., Egeblad, H. and Saltin, B (1984). Static contraction of the quadriceps muscle in man: cardiovascular control and responses to one-legged strength training. Acta Physiologica Scandinavia, 122, 341-353
37. Lind, A.R. and McNichol, G.W (1967). Muscular factors which determine the cardiovascular responses to sustained and rhythmic exercise. Canadian Medical Association Journal, 96, 706-715
38. Little, W.C, Constantinescu, M., Applegate, R.J, Kutcher, M.A., Burrows, M.T., Kahl, F.R. and Santamore, W.P (1988). Can coronary angiography predict the site of a subsequent myocardial infarction in patients with mild to moderate coronary artery disease?. Circulation, 78, 1157-1166
39. Little, W.C., Gwinn, N.S., Burrows, M.T., Kutcher, M.A., Kahl, FR. and Applegate, R.J (1990). Cause of acute myocardial infarction late after successful coronary artery bypass grafting. American Journal of Cardiology. 65, 808-810
40. Mitchell, J.H., Payne, F.C., Saltin, B. and Schibye, B (1980). The role of muscle mass in the cardiovascular response to static contractions. Journal of Physiology, 309, 45-54
41. O'Connor, G.T., Buring, J.E., Yusuf, S., Goldhaber, S.Z., Olmstead, E.M., Paffenbarger, R.S. Jr. and Hennekens, C.H (1989). An overview of randomized trials of rehabilitation with exercise after myocardial infarction. Circulation, 80, 234-244
42. Oldridge, N.B. and Rogowski, B.L (1990). Self-efficacy and in-patient cardiac rehabilitation. American Journal of Cardiology, 66, 362-365
43. Oldridge, N.B., Guyatt, G.H., Fisher, M.E. and Rimin, A.A (1988). Cardiac rehabilitation after myocardial infarction: combined experience of randomized clinical trials. Journal of the American Medical Association, 260, 945-950
44. Omish. D., Brown, S.E., Sherwitz, L.W., Billings, J.H., Armstrong, W.T., Ports, T.A., McLanahan, S.M., Kirkeeide, R.L., Brand, R J. and Gould, K.L (1975). Can lifestyle changes reverse coronary heart disease?. The Lifestyle Heart Trial. Lancet, 446, 129-133
45. Pandolf, K.B., Cafarelli, E. and Noble, B.J (1975). Hyperthermia: effect en exercise prescription. Archives of Physical Medicine and Rehabilitation, 56, 524-526
46. Savin, W.M., Haskell, W.L., Houston-Miller, N. and DeBusk, RE (1981). linprovement in aerobic capacity soon after myocardial infarction. Journal of Cardiac Rehabilitation, 1, 337-342
47. Shcldahl, L.M., Wilke, N.A., Tristaiii, F.E. and Hughes, C.V (1984). Heart rate responses during home activities soon after myocardial infarction. Journal of Cardiac Rehabilitation, 4, 327-333
48. Simoons, M.L., Serruys, P.W., van den Brand, M., Res, J., Verheugt, FW., Krauss, X.H., Recome, W.J., B5r, E, de Zwaan, C. and Van der Laarse, A (1986). Early thrombolysis in acute myocardial infarction: limitation of infarct size and improved survival. Journal qf the Amen can College of Cardiology, 7, 717-728
49. Smith, S.C (1996). Risk-reduction therapy: The challenge to change. Circulation, 93,2205-2211
50. Smith, S.C., Blair, S.N., Cniqui, M.H., Fletcher, G.F., Fuster, V., Gersh, B.J., Gotto, A.M., Gould, K.L., Greenland, P. and Grundy, S.M (1995). Preventing heart attack and death in patients with coronary disease. Circulation, 92, 2-4
51. Superko, H.R. and Krauss, R.M (1994). Coronary artery disease regression: Convincing evidence for the benefit of aggressive lipoprotein management. Circulation, 90, 1056-1069
52. Tran, Z.V. and Brammell, H.L (1989). Effects of exercise training en serum lipid and lipoprotein levels in post-MI patients. A meta-analysis. Journal of Cardiopulmonary Rehabilitation, 9, 250255
53. Van Camp, S.P.R and Peterson, R.A (1986). Cardiovascular complications of outpatient cardiac rehabilitation programs. Journal of the American Medical Association, 256, 1160-1163
54. Weiner, D.A., McCabe, C.H., Roth, R.L., Cutler, S.S., Berger, R.L and Ryan, T.J (1981). Serial exercise testing after coronary bypass surgery. American Heart Journal, 101, 149-154
55. Wenger, Froelicher, Smith, Ades, Berra, Blumenthal, Certo, Dattilo, Davis, DeBusk, Drozda, Fletcher, Franklin, Gaston, Greeland, McBride, McGregor, Oldridge, Piscatella and Rogers (1995). Cardiac rehabilitation as secondary prevention. Clinical practice guideline. Quick reference guidefor clinicians, No. 17. AHCPR Publication No. 96-0673
56. Williams, R.B., Califf, R.M., Barefoot, J.C., Haney, T.L., Saunders, W.B., Pryor, D.B., Hlatky, M.A., Siegler, I.C. and Mark, D.B (1992). Prognostic importance of social and economic resources among medically treated patients with angiographically documented coronary artery disease. Journal of the American Medical Association, 267, 520-524
57. Winslow, E.H (1985). Cardiovascular consequences of bed rest. Heart & Lung, 14, 236-246
58. World Health Organization Expert Committee (1964). Rehabilitation of patients with cardiovascular diseases. Technical report series no. 270. Geneva: World Health Organization
59. World Health Organization Expert Committee (1993). Rehabilitation after cardiovascular diseases, with special emphasis en developing . No Disponible