Efectos de un Suplemento Comercial Termogénico para la Pérdida de Peso sobre la Composición Corporal y el Gasto Energético en Adultos Obesos
Jeffrey W Armstrong1, Patrick Johnson1 y Simone Dume1
Department of Health, Physical Education, Recreation, and Dance, Ruth Bouhner Applied Physiology Laboratory, Eastern Michigan University, Ypsilanti, MI 48197.
Artículo publicado en el journal PubliCE, Volumen 0 del año 2001.
Publicado 4 de enero de 2003
Resumen
Palabras clave: colesterol, dexa, gasto energético, efedrina, ejercicio, glucosa
INTRODUCCIÓN
La obesidad se esta volviendo cada vez más común en los Estados Unidos (5). Debido a que es un factor de riesgo establecido, para la hipertensión, diabetes miellitus no insulino dependiente, hiperlipidemia, y arterioesclerosis, es imperativo encontrar un tratamiento para esta enfermedad. La obesidad es habitualmente considerada como un producto de la inactividad y la sobrealimentación. Sin embargo un análisis simple de la obesidad, falla al considerar interacciones más complejas que dependen de esta enfermedad, como factores genéticos, psicológicos, y conductuales. La obesidad también puede incluir una disminución de la regulación del sistema nervioso simpático sobre la termogénesis (15).
Investigaciones recientes indicaron que la efedrina, un componente simpático, puede tener algunas propiedades anti-obesidad (1). Ha sido demostrado que incrementa el gasto energético en humanos (1, 14) y en monos (13). Cuando se combina con cafeína y una dieta restringida, podría tener un efecto constante en el mejoramiento y mantención de la composición corporal (3, 6, 13, 16). Daly y cols. sostuvieron una estrategia de combinación de bajas dosis de efedrina, cafeína, y aspirina para una estimulación simpática de la termogénesis (6). Se piensa que grandes dosis de efedrina podrían presentar riesgos sustanciales para los pacientes (2, 4, 7, 8, 9). Los riesgos reportados incluyen cálculos en el nefrón (2), disturbios psiquiátricos (9), síntomas maniacos (7), agarrotamiento, problemas cardiovasculares, y hasta la muerte (4). Por ello, bajas dosis de varios agentes pueden reducir la toxicidad (6).
La efedrina incrementa la liberación de norepinefrina (NE) desde la terminal del nervio simpático. Por más que los niveles de NE se incrementan, la respuesta termogénica puede ser limitada por la liberación de adenosina y prostaglandinas (PG) desde otros tejidos estimulados, que actúan como inhibidores (6). La cafeína y la aspirina pueden evitar estas inhibiciones por la antagonización de la adenosina y de las fosfodiesterasas e inhibiendo la síntesis de PG, respectivamente, y de esta manera incrementar y sostener la activación de las células efectoras (6).
La efedrina puede afectar el apetito. Se ha reportado que disminuye el consumo de comida en monos obesos (13). Daly y cols. (6), por contrapartida, no observaron diferencias en el apetito reportado por los sujetos que tomaron una combinación de efedrina, cafeína y aspirina. Asimismo Pasquali y cols. (11) notaron una falta de efecto anorexígeno. Ninguno de estos grupos, sin embargo, reportaron ningún análisis estadístico.
El propósito del siguiente estudio fue examinar los efectos de una preparación particular, disponible comercialmente (Xenadine RFA-1, Cytodyne Technologies, Lakewood, NJ) que contiene ma huang, un derivado botánico de la efedrina, y extracto de guaraná (cafeína) sobre la composición corporal, el gasto energético en reposo, y el apetito mientras se combinan con una moderada actividad física.
MÉTODOS
Sujetos
Veintiséis sujetos (20 mujeres y 6 varones) fueron reclutados del staff de estudiantes de la Universidad de Michigan del Este y de la comunidad aledaña mediante carteles, volantes y avisos en el periódico universitario. Los sujetos fueron equiparados de acuerdo a la edad, sexo, altura, peso y grasa corporal y fueron asignados aleatoriamente para recibir la suplementación (Suplementación n =13) o un placebo (Placebo n=13) de acuerdo con el orden de las dosis explicadas más abajo. Seis participantes (5 mujeres y 1 varón) dejaron el estudio por múltiples razones. Un varón (Placebo) y una mujer (Suplementación) decidieron retirarse debido a los posibles efectos colaterales. Los restantes (4 mujeres, Placebo) dejaron el estudio por razones que no comentaron. Debido a esto, un total de 20 sujetos completaron el estudio (Suplementación n =12; Placebo n =8). Todos eran aparentemente saludables, y libres de contraindicaciones para realizar ejercicios como se determinó a través de una historia clínica. Se obtuvo un consentimiento escrito de los sujetos antes de la participación y el Comité de Revisión de la Universidad de Michigan aprobó todos los procedimientos. Las características de los sujetos se encuentran en la Tabla 1, los criterios de inclusión/exclusión son listados en la Tabla 2.

Tabla 1. Características Físicas de los Sujetos (media ± DS)

Tabla 2. Criterios de Inclusión y Exclusión.
Tratamiento
El suplemento, Xenadrine RFA-1 (Cytodyne Technologies, Lakewood, NJ) y el placebo fueron de las mismas características y distribución (Tabla 3). Para los primeros dos días de suplementación los sujetos tomaban una cápsula antes del desayuno (aproximadamente 8-9 AM) y una cápsula antes de la merienda (aproximadamente 2-3 PM). Posteriormente, el número de cápsulas se incrementó a dos para el consumo de la mañana y la tarde durante los 44 días.

Tabla 3. Contenido de Ingredientes del Suplemento y el Placebo (por dos
cápsulas)
Evaluaciones
Se realizó una sesión para la pre y pos evaluación respectivamente. En la mañana del día de las evaluaciones, los sujetos llegaron al laboratorio de fisiología aplicada entre las 6 y 10 AM. Los participantes descansaron en posición supina, quietos con los ojos cerrados sobre una camilla en una habitación tranquila por 10-15 min. Después de este periodo se les colocó una boquilla, los gases espirados fueron colectados durante 5 minutos, y el gasto energético diario en reposo (REE) fue determinado durante 5 minutos utilizando un circuito espirométrico abierto (VO2 máx., Sensormedics, Yorba Linda, CA) y fue reportado relativo al peso corporal (kcal/kg/d). La frecuencia cardiaca, la presión sanguínea, y el electrocardiograma fueron evaluados como medidas de precaución y no fueron analizadas estadísticamente.
Después de la medición de REE, 5 ml de sangre fueron extraídos por punción venosa de la vena cubital anterior del dorso de la mano. El suero fue separado y en el Laboratorio Clínico de la Universidad de Michigan, se analizó glucosa (GLU), colesterol (CHOL), triacilglicéridos (TRIG), y lipoproteínas de alta intensidad (HDL). El colesterol de las lipoproteínas de baja densidad fue calculado utilizando la siguiente ecuación:
LDL =CHOL-HDL-(TRIG/5).
La composición corporal fue evaluada durante la tarde siguiente, mediante DEXA (Prodigy model, Lunar Radiation Corporation, Madison, WI) en el laboratorio del Departamento de Radiología del Hospital St Joseph Mercy en Ypsilanti, Michigan por técnicos entrenados bajo la supervisión de los médicos. El DEXA proveyó datos de la masa corporal total (BM), porcentaje de grasa (%grasa), masa grasa (FM), y masa magra (FFM). El DEXA provee información precisa analizando tres compartimientos, con una baja exposición de los sujetos a la radiación (10). Es considerada una herramienta útil para la medición de la composición corporal (10,12) con una precisión de error para la densidad mineral ósea (BMD), % de grasa, FM, y FFM menor a 0.01 g/cm2, 1.4%, 1.0 kg, y 0.8 kg, respectivamente (10).
Debido a que se propuso que el suplemento en estudio posee un efecto en la supresión del apetitito, se les pidió a los sujetos que tomen nota durante 3 días de su dieta durante una semana común. Como resultado de una limitada adherencia los datos pre y pos test estuvieron disponibles solo para 14 sujetos (Suplementación =9, Placebo = 5). Los datos fueron analizados como la media de los 3 días en calorías totales (Kcal), proteínas totales (PROT); carbohidratos totales (CHO), y grasas totales (GRASA) utilizando un Sofware Nutricional Library TM (Compunutrition, Chatsworth, CA.)
Protocolo de Entrenamiento
El ejercicio aeróbico fue conducido en un circuito interno de la Universidad de Michigan durante una de las tres sesiones monitoreadas (6-9 AM, 11 AM a 1PM, o 5-7 PM). La primer semana después del pre-test consistió en dos caminatas de pre-acondicionamiento de 2.4 km a un paso confortable (activo pero no exhaustivo). Esta distancia fue incrementada a 3.2 km tres veces por semana, permitiendo a los sujetos realizar un pequeño trote si así lo deseaban. Si los sujetos no podían asistir a las sesiones, se les permitía realizar una sesión independientemente. Debido a que estas sesiones no pudieron ser monitoreadas, los investigadores aceptaban la palabra de los sujetos como prueba que la sesión fue realizada.
Análisis de los Datos
El programa estadístico SPSS versión 10.0 de Windows fue utilizado para todos los análisis estadísticos. Las diferencias entre pre y pos test de REE relativo al peso corporal (REE/BM), BM, %de grasa, FM, y FFM fueron comparados utilizando un test-t independiente. Los datos de 3 días de dieta y los parámetros bioquímicos sanguíneos fueron analizados realizando mediciones repetidas de doble MANOVA para determinar, ya sea, si existieron efectos significativos de tiempo y grupo para una combinación lineal de variables dependientes. Los datos se presentan como medias ± D.S. y el test-t de Student fue utilizado para comparar las diferencias iniciales de edad, BM, altura, y % de grasa. Además, los efectos del tamaño para las variables dependientes fueron calculados basados bajo las medias y DS obtenidas a partir de los datos del pre y pos tratamiento de suplementación (Tabla 4). La significancia fue seleccionada a un nivel alfa de 0.05 para todos los análisis.
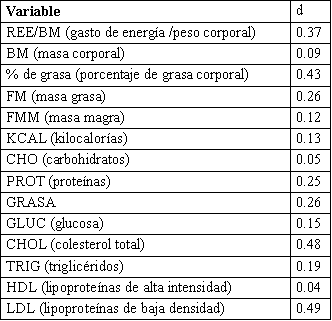
Tabla 4. Efectos del tamaño (d) para las Variables Dependientes
RESULTADOS
Datos Pre-Entrenamiento
La media (± DS) de la edad, altura, peso corporal, y porcentaje de grasa fueron 31.0 ± 7.5 años, 168.3 ± 8.4 cm, 93.4 ± 17.1 kg, y 43.8 ± 6.5%, respectivamente. Además el grupo Placebo fue escasamente mas alto, pesado y magro que el grupo suplementado (Tabla 1), los grupos no se diferenciaron significativamente al inicio del estudio (p =0.769, 0.117, 0.577 y 0.421, respectivamente).
Mediciones de Composición Corporal y REE
Los datos pre y pos suplementación de REE/BM y composición corporal para ambos grupos son mostrados en la tabla 5. Los test-t independientes revelaron que la única diferencia significativa entre grupos en alfa <0.05 fue FM (p = 0.688, 0.087, 0.096, 0.033, 0.554 para REE/BM, BM, % de grasa, FM, FFM, respectivamente).
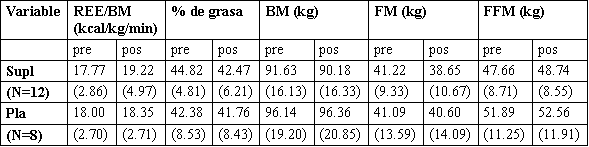
Tabla 5. Promedios de las Mediciones del Gasto Energético y Composición
Corporal (± DS)
Análisis de la Dieta
Los datos de la dieta pre y pos-suplementación para ambos grupos son mostrados en la Tabla 6. Utilizando MANOVA, no se hallaron cambios significativos en la dieta de los sujetos durante el periodo de suplementación (p =0.129), tampoco hubo diferencias significativas entre grupos, en KCAL, PROT, CHO y GRASAS combinadas (p =0.622).
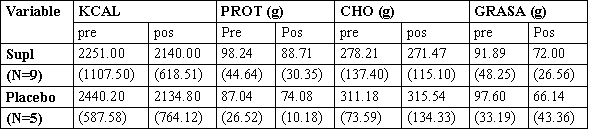
Tabla 6. Promedios de Ingesta Dietaria (±DS)
Bioquímica Sanguínea
Los datos pre y pos-suplementación de la bioquímica sanguínea para cada grupo son mostrados en la Tabla 7. Utilizando MANOVA, no hubo cambios significativos en la bioquímica sanguínea de los sujetos durante el período de suplementación (p =0.094), y no hubo diferencias significativas entre grupos para GLUC, CHOL, TRIG, HDL y LDL combinados (p =0.775).
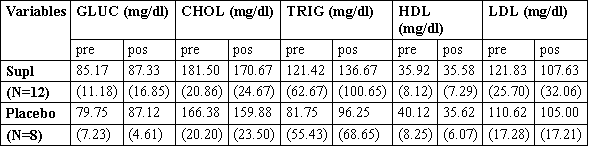
Tabla 7. Promedio de las Mediciones de la Bioquímica Sanguínea (± DS)
DISCUSIÓN
El presente estudio fue iniciado para establecer si seis semanas de suplementación con un suplemento termogénico para la pérdida de peso, disponible comercialmente (Xenadrine RFA-1) pueden afectar la composición corporal, el apetito, y el gasto energético de reposo en hombres y mujeres obesos. Investigaciones previas indicaron que la efedrina proveniente de una fuente botánica (ma huang) incrementa el gasto energético de reposo en monos obesos (13) y humanos (1, 12). Asimismo, se ha reportado que la efedrina facilita la pérdida de peso en monos obesos (13). Cuando se combina con cafeína los efectos son aparentemente mejores (16). También ha sido propuesto el agregado de aspirina (6).
El suplemento, Xenadrine RFA-1, es estandarizado para dosis de 20 mg de efedrina botánica (ma huang) y 200 mg de cafeína (extracto de guaraná) para una dosis de 2 cápsulas. Según Gurley et al. (8), la farmacocinética de la efedrina botánica es similar a la sintética. Por ello el contenido de ma huang dentro de este producto es similar al usado en los tratamientos revisados. Cuando se analizaron los efectos de la efedrina sin combinación, las dosis fueron 10, 20 y 40 mg (1), 25 y 50 mg (11), o 50 mg tres veces al día (14). Las dosis combinadas de efedrina y cafeína fueron 20 mg y 200 mg (16). En contraposición a los estudios previos Xenadrine RFA-1 contiene un agente simpatoadrenérgico adicional, naranja amarga (estandarizada para 5 mg de sinefrina).
Se esperaba que la dosis ingerida pudiera promover cambios en la composición corporal. El único cambio de significancia estadística fue FM (p = 0.033). Hubo, sin embargo, una modesta caída en BM y en el % de grasa para los sujetos que tomaron el suplemento (p =0.087 y 0.096 respectivamente). Esto es comparable a los datos de Daly y cols. (6) quienes reportaron una media acumulada significativamente mayor en la perdida de peso en sujetos que tomaron una combinación de efedrina/cafeína/aspirina (-1.8 kg vs. 0.5 kg). Estos cambios pudieron haber sido desequilibrados por aumentos en la variable FFM (-2.38 kg a + 4.0899). Todos excepto 4 sujetos perdieron masa grasa (1 Suplementación y 3 Placebo), mientras que solo 12 sujetos ganaron masa magra (7 Suplementación y 5 Placebo o 53.8% y 62.5% respectivamente). Por lo tanto mientras el suplemento puede promover pérdida de grasa, sus efectos sobre la masa magra son controvertidos.
El hecho de que el gasto de energía relativo al peso corporal no aumento
durante el periodo de suplementación puede no estar de acuerdo con estudios
previos. Shanon y cols. (14) observaron un incremento en el promedio del gasto
de energía durante 24 hs., pero no en la tasa metabólica basal determinada
entre 6.30 y 7.30. Esta medición fue realizada de 11 a 12 horas después de la
última toma de efedrina. En el presente estudio, el gasto de energía de reposo
fue determinado después de un periodo de tiempo mucho mayor. Los sujetos
ingirieron su última dosis en la tarde previa a la evaluación, la cual fue
programada entre las 6:00 y 10:30 hs. Este puede haber sido suficiente tiempo
para reducir los efectos de la suplementación.
También debe considerarse que el método usado para medir el REE no esta exento
de limitaciones. Respirar a través de una boquilla permite solo una pequeña
muestra de gases mientras el sujeto esta despierto, pero relajado. Además en
tales condiciones un aparato respiratorio puede afectar la actividad simpática
(14). Idealmente la cámara metabólica podría ser usada para un muestreo
extendido.
Los análisis de glucosa, colesterol, triglicéridos, colesterol HDL y colesterol LDL, no revelaron efectos de la suplementación. Esto coincide con los resultados reportados por Daly y cols. (6). Estos investigadores, no observaron cambios en la glucosa, insulina, colesterol LDL y colesterol HDL, después de 8 semanas de suplementación con una mezcla de efedrina, cafeína y aspirina. Mientras que aparentemente, no hay beneficios sobre esos componentes sanguíneos, puede notarse que no hubo efectos negativos observados en la sangre.
Los análisis de la dieta también fallaron en indicar algún efecto sobre la ingesta de energía, proteínas, carbohidratos o grasas. Esto concuerda con Daly y cols. (6) quienes tampoco observaron diferencias significativas en el reporte individual del apetito de los sujetos. Sin embargo la adherencia fue un problema. De 20 sujetos estudiados, solo 7 completaron todas las anotaciones requeridas. Con el objeto de maximizar la eficiencia de la observación solo se analizaron los datos de la pre y pos-suplementación (n =14).
Otra consideración respecto a la falla en encontrar cambios en el apetito, es que los datos de la comida consumida pueden no ser suficiente medida del hambre en la obesidad. La obesidad incluye complejos factores psicológicos, así como factores fisiológicos y conductuales. En conclusión del estudio, un sujeto expresó conciencia de un patrón de desorden alimentario. Horarios y actividades diferentes pueden afectar cuanto fue comido día a día y sujeto a sujeto. La cantidad de comida consumida también puede estar relacionada a hábitos o a necesidades emocionales más que a necesidades físicas. Por lo tanto se deberían considerar diferentes mediciones para evaluar el apetito.
Efectos Colaterales
Mientras que los efectos colaterales no fueron evaluados directamente, se puso especial atención a cualquier efecto adverso de la suplementación. De los sujetos que comenzaron con el suplemento, solo dos sintieron alguna molestia. Una mujer reportó un aumento en la ansiedad y un incremento en la frecuencia cardiaca durante los primeros días del estudio. Estos síntomas pasaron pronto y la mujer continuo sin molestias. Una mujer, sin embargo, dejó el estudio debido a que estaba molesta con la elevada frecuencia cardiaca y con un sentimiento de "sangre caliente". Las reacciones a estos productos como el evaluado en este estudio, son comunes. Los investigadores han reportado previamente efectos colaterales en algunos sujetos como, boca seca, temblores, y constipación (1, 6, 11, 16), dolor de cabeza e insomnio (11, 16), mientras que en otros han reportado efectos colaterales mas severos como vómitos, dolor abdominal, y temblor (3), cálculos en el riñón (2), desordenes psicológicos (7, 9), agarrotamiento, problemas cardiovasculares y la muerte (4). De los estudios revisados, sin embargo solo Cupps (4), Gurley y cols. (8), y Jacobs y Hirsch (9) hablan de la efedrina botánica (ma huang). En muchos de los casos, los síntomas son pocos severos y desaparecen dentro de un mes. Gurley y colaboradores (8) sugirieron que los casos severos de la toxicidad de ma huang tienden a estar asociados con el abuso del suplemento. Por lo tanto, se debe acentuar la atención sobre las precauciones de los fabricantes y sobre síntomas inusuales.
Confianza Estadística
Los efectos de las variables dependientes (Tabla 4) son de pequeños a moderados (0.09 a 0.49). Por lo tanto, la habilidad de detectar diferencias reales a través de una muestra pequeña es limitada. La habilidad para detectar cambios en REE/BM, % de grasa, y FM en particular pudo haber sido disminuida. Dados estos efectos del tamaño (d = 0.37, 0.43 y 0.26, respectivamente), es requerido, un tamaño de muestra que exceda los 90 sujetos por grupo para obtener una potencia mínima de 0.80 (17). Además, son necesarios controles más severos sobre el análisis de la dieta y mediciones del apetito.
Sugerencias para Futuras Investigaciones
Mientras que este estudio indico efectos positivos de la suplementación con efedrina /cafeína sobre el peso corporal y el porcentaje de grasa, se necesitan más investigaciones similares a esta, para examinar mas claramente la seguridad y la eficacia de un suplemento termogénico para la pérdida de peso corporal. Puede ser necesario un periodo de entrenamiento mas largo. Toubro y cols. (16) observaron perdidas significativas del peso corporal en sujetos tratados con efedrina mas cafeína, sólo después de la octava semana. También se recomiendan mediciones mas precisas del gasto energético durante periodos de tiempo más largos. Los datos de la dieta deberían ser analizados con mayor severidad y se debería incluir alguna medición de los niveles de apetito.
Referencias
1. Astrup A, Soubro S, Cannon S, Hein P, Madsen J (1990). Thermogenic, metabolic, and cardiovascular effects of a sympathomimetic agent, ephedrine. Curr Ther Res; 48(6):1087-1100
2. Blau JJ (1998). Ephedrine nephrolithiasis associated with chronic ephedrine abuse. J Urol; 160:825
3. Cupps MJ (1999). Herbal remedies: adverse effects and drug interactions. Am Fam Physician; 59(5):1239-1244
4. Dalton S (1997). Overweight and weight management: the health professionals guide to understanding and practice. Gaithersburg: Aspen Publishers, Inc
5. Daly PA, Krieger DR, Dulloo AG, Young JB, Landsberg L (1993). Ephedrine, caffeine and aspirin: safety and efficacy for treatment of human obesity. Int J Obesity; 17(Suppl. 1):S73-S78
6. Emmanuel NP, Jones C, Lydiard, RB (1998). Use of herbal products and symptoms of bipolar disorder. Am J Psychiatry; 155(11):1627
7. Gurley BJ, Gardner SF, White LM, Wang P-L (1998). Ephedrine pharmokinetics after ingestion of natural supplements containing Ephedra sinica (ma huang). Ther Drug Monit; 20:439-445
8. Jacobs KM, Hirsch KA (2000). Psychiatric complications of ma-huang. Psychosomatics; 41(1):58-62
9. Mazess RB, Barden HS, Bisek JP, Hanson J (1990). Dual-energy x-ray absortiometry for total-body and regional bone mineral and soft-tissue composition. Am J Clin Nutr; 51:1106-1112
10. Pasquali R, Baraldi G, Cesari MP, Melchionda N, Zamboni M, Stefanini C, Raitano A (1985). A controlled trial using ephedrine in treatment of obesity. Int J Obesity; 9:93-98
11. Pierson RN, Wang J, Heymsfield SB, Russell-Aulet M, Mazariegos M, Tierney M, Smith R, Thornton JC, Kehayias J, Weber DA, Dilmanian (1991). Measuring body fat: calibrating the rulers. Intermethod comparisons in 389 normal Caucasian subjects. Am J Physiol; 261:E103-E108
12. Ramsey JJ, Colman RJ, Swick AG, Kemnitz JW (1998). Energy expenditure, body composition, and glucose metabolism in lean and obese rhesus monkeys treated with ephedrine and caffeine. Am J Clin Nutr; 68:42-51
13. Shannon JR, Gottesdiener K, Jordan J, Chen K, Flattery S, Larson PJ, Candelore MR, Gertz B, Robertson D, Sun M (1999). Acute effect of ephedrine on 24-h energy balance. Clin Sci; 96:483-491
14. Spraul M, Ravussin E, Fontvieille AM, Rising R, Larson DE, Anderson EA (1993). Reduced sympathetic nervous system activity. A potential mechanism predisposing to body weight gain. J Clin Invest; 92 (4):1730-1735
15. Toubro S, Astrup A, Breum L, Quaade F (1993). Safety and efficacy of long-term treatment with ephedrine, caffeine and an ephedrine/caffeine mixture. Int J Obesity; 17(Suppl. 1):S69-S72
16. Vincent WJ (1999). Statistics in Kinesiology, 2nd ed. Champaign, IL: Human Kinetics