Escuela Internacional Educación Física y Deportes.
Resumen
INTRODUCCIÓN
La respuesta del organismo a los esfuerzos de alta intensidad sigue siendo un aspecto que causa preocupación en la comunidad científica, así como entre los entrenadores y deportistas. A diferencia de otro tipo de esfuerzos, submáximos o de menor intensidad, en los máximos existe una gran limitación por cuanto se pueden mantener durante períodos cortos de tiempo, estando asociado su cese a corto plazo a la fatiga muscular, especialmente de los músculos implicados en el ejercicio, lo cual genera disfunciones y molestias que culminan con la parada el ejercicio.
Los mecanismos que producen fatiga muscular luego de una serie de ejercicios son pobremente conocidos y pueden involucrar una disminución de la conducción nerviosa (Bigland & Ritchie 78´), una falla en los sitios de excitación – contracción (Bigland & Ritchie 74´ – Enoka & Stuart 92´) o ciertas consecuencias metabólicas como el descenso de la fosfocreatina (PC) intramuscular o el incremento de lactato y la disminución del pH (Chasiotis 83´- Hirvonen 87´- Hultman 90´- Spriet 87´).
La fatiga muscular se manifiesta por un descenso de la capacidad de generar fuerza o potencia y se da en contracciones máximas o submáximas. Está definida como «una incapacidad para mantener los requerimientos o la fuerza generada» (Edwards, 1981), y provocada, en parte, por un descenso del pH intramuscular (Costill y Cols. 1988), así como por una serie de disturbios en los electrolitos de los músculos (McKenna, 1992).
DESARROLLO
La contracción muscular intensa está acompañada de un incremento del contenido de agua del músculo distribuido en los espacios intra y extracelulares. Esta afluencia de agua puede modificar la concentración de iones en ambos compartimentos. El resultado de estos cambios en la concentración iónica intracelular motivados por el ejercicio físico intenso, será una reducción de la diferencia de concentración de iones, con el consiguiente aumento de la concentración de iones de hidrógeno intracelular, produciendo acidosis (McKenna, 1992). Esta acidosis influye de forma clara en la fatiga muscular, afectando la función contráctil proteínica, la regulación del calcio y el metabolismo muscular. Por otra parte, y dado que las demandas metabólicas del ejercicio de alta intensidad son cubiertas predominantemente mediante la degradación anaeróbica de la glucosa, este proceso produce ácido láctico, por lo que ocurre el consecuente descenso del pH de los músculos que se ejercitan (Edington y cols., 1976). La fatiga muscular, pues, está asociada entre otros aspectos, a un rápido incremento en la producción de ácidos metabólicos. La tolerancia al ejercicio de alta intensidad puede estar limitada por la capacidad del organismo para amortiguar el descenso del pH intracelular (músculo) y extracelular (sangre), esto es, el sistema buffer intrínseco. En definitiva, los esfuerzos máximos producen un desequilibrio ácido-base en el organismo, ante lo cual éste posee intrínsecamente una capacidad para luchar contra la acidosis, esto es el sistema buffer o de amortiguación.
¿Ácido o base?
Que una solución sea ácida o alcalina depende de la concentración de iones hidrógeno (H+). Si la concentración de iones hidrógeno está aumentada, la solución se vuelve más ácida; si la concentración está disminuida, se vuelve más alcalina. La cantidad de hidrógeno ionizado en una solución está indicada por el concepto de pH. En el laboratorio, una solución con un pH de 7 es neutra, a esa concentración el número de iones hidrógeno está equilibrado por el número de iones hidroxilo presentes. A medida que la concentración de ión hidrógeno cae, el valor del pH se eleva. En otras palabras, una solución ácida tiene un valor de pH inferior a 7 y una solución alcalina tiene un valor de pH mayor que 7.
En los seres humanos, el líquido extracelular normalmente es levemente alcalino, con un pH de 7,35 a 7,45. Si el pH se eleva más que esto, existe un estado de alcalosis; si el pH cae por debajo de este valor, existe un estado de acidosis. En el estado de acidosis, aún el líquido corporal puede considerarse alcalino, aunque menos que lo normal. Si el pH del líquido corporal se eleva por encima de 7,7 o cae por debajo de 7, la vida de la persona está en peligro.
El metabolismo normal del cuerpo produce continuamente radicales ácidos. Esta producción se incrementa durante los ejercicios de máxima intensidad. Los mecanismos de defensa inmediatos, para evitar cambios en el pH en respuesta a modificaciones en la acidez de los líquidos corporales, son realizados por los sistemas amortiguadores (buffers) del cuerpo, además de la regulación respiratoria y la regulación renal del pH.
Pero veamos a continuación en qué se basa la clasificación de sustancias ácidas o básicas.
De acuerdo con Brönsted, un ácido es una sustancia con la capacidad para donar iones de H+ y una base es un compuesto con la capacidad para aceptar o captar iones de H+.
¿Que es el pH?
El pH de una solución se define, de acuerdo a los conceptos de Sorensen, como el logaritmo inverso de la concentración de hidrogeniones: pH = log1/ [H+] = -log [H+]
Sistemas de amortiguación del equilibrio ácido-base: El sistema buffer
Una solución buffer es aquella que tiende a absorber el exceso de iones hidrógeno o a liberarlos según la necesidad. Por eso es importante en la regulación del equilibrio ácido-base en los líquidos corporales. Aunque existen tres sistemas buffers importantes, el sistema buffer del bicarbonato es el más significativo, porque el cuerpo puede alterar las concentraciones relativas de ácido carbónico y bicarbonato de sodio.
Cuando cualquier ácido más fuerte que el ácido carbónico ingresa a la sangre, es amortiguado por la reacción con la sal de bicarbonato de sodio. Los iones hidrógeno son eliminados para formar moléculas de ácido carbónico y una sal de sodio ácida más fuerte. Veamos nuestro ejemplo.
Ácido láctico + Bicarbonato de sodio → Lactato de sodio + Ácido carbónico
Un trastorno del equilibrio ácido-base puede considerarse el resultado de desequilibrio en el sistema ácido carbónico / bicarbonato de sodio (o alguna otra base). Estos bicarbonatos se hallan en el líquido extracelular en una relación 1/20 de ácido carbónico y el bicarbonato básico. El equilibrio ácido-base y el pH normal del líquido corporal cambian cuando esta relación está alterada.
En la situación clínica, el equilibrio o desequilibrio ácido-base puede determinarse a partir del pH sérico, de la presión parcial del C02 y los niveles de bicarbonato. El pH sanguíneo puede medirse incluso con pequeñas muestras de sangre. Los valores normales de pH están entre 7,35 y 7,45, como ya hemos mencionado anteriormente. La concentración de ácido carbónico (H2CO3) es cuantitativamente despreciable en comparación con el dióxido de carbono disuelto. El valor normal es aproximadamente 40 mm Hg.
Regulación respiratoria
A medida que la profundidad y la frecuencia respiratoria aumentan, con el ejercicio, se pierde más dióxido de carbono, disminuyendo la concentración de ácido carbónico en la sangre. A medida que la profundidad y frecuencia respiratoria disminuyen (respiración superficial), se extrae menos dióxido de carbono y la concentración de ácido carbónico en la sangre está aumentada, lo que conduce a un cambio en la relación de ácido carbónico con bicarbonato de sodio. Los pulmones deben tener tejido elástico normal para que se produzca la remoción eficiente de dióxido de carbono. Cualquier trastorno que disminuya esta elasticidad produce retención de dióxido de carbono y ácido carbónico, conduciendo a la acidosis con un pH menor que el normal.
Aunque los pulmones pueden modificar el pH cambiando la PCO2 y alterando la relación de ácido carbónico con bicarbonato, no existe ningún cambio en la cantidad de iones hidrógeno. Los pulmones no pueden regenerar bicarbonato para reemplazar lo que se ha perdido cuando los iones hidrógeno fueron amortiguados. La formación de nuevo bicarbonato y la excreción de bicarbonato, si es necesario, son funciones de los riñones.
Regulación renal del pH
Su acción tarda más que las anteriores pero es la más potente y es muy importante para conservar la reserva alcalina del cuerpo. El ácido carbónico se forma en las células tubulares del riñón a través del siguiente proceso: cuando se forma el dióxido de carbono durante la actividad celular en el Ciclo de Krebs, se combina con agua bajo la influencia de la anhidrasa carbónica, como en otras células, y se forma el ácido carbónico. Un ión hidrógeno del ácido carbónico entra al filtrado en intercambio por un ión sodio. El ión hidrógeno reemplaza entonces al sodio en la molécula de fosfato y es excretado en la orina. El H3CO2 en el filtrado no se pierde totalmente en la orina porque el ácido carbónico se divide en CO2, y agua. El dióxido de carbono difunde hacia atrás a la célula tubular y vuelve a los capilares como bicarbonato de sodio o ión bicarbonato.
Un segundo medio utilizado por la célula tubular para regular el pH es la secreción de amoníaco. La glutamina es metabolizada, de lo que resulta NH3, cuando la acidez de los líquidos corporales es baja. Cuando el amoníaco ingresa al filtrado, vuelve un ión sodio a la célula tubular y luego a los capilares. Si los líquidos corporales no son ácidos, no se produce la secreción de amoníaco.
Los iones hidrógeno y el amoníaco son secretados en intercambio por sodio en el filtrado. Esto produce el regreso del bicarbonato de sodio a la sangre. Existe un incremento entonces, en la fracción de bicarbonato del par buffer ácido carbónico / bicarbonato de sodio.
La regulación del pH se vuelve progresivamente más difícil cuando los iones de hidrógeno aumentan por la producción de CO2 y ácido láctico, como ocurre en el caso de realizar un ejercicio de alta intensidad, donde la vía de producción de energía es predominantemente anaeróbica. Es entonces cuando la perturbación del equilibrio ácido-base de los músculos se considera uno de los factores limitantes del rendimiento. El mecanismo por el que la acidosis intracelular produce fatiga aún no está claro, si bien podría deberse a la inhibición de los procesos de contracción del músculo y de enzimas glucolíticas perjudicando la resíntesis de ATP.
La Acidosis Láctica severa
El ácido láctico es un producto terminal del metabolismo anaeróbico de la glucosa y se obtiene por reducción del ácido pirúvico en una reacción catalizada por la enzima deshidrogenasa láctica donde interviene como coenzima la nicotinamida adenina dinucleótido (NAD) que pasa de su forma reducida a la forma oxidada. En condiciones normales, los niveles séricos alcanzan los 2 mEq/L o menos, pero el ejercicio puede elevarlo hasta 4 mEq/L. La mayor parte del lactato se elimina de forma muy eficaz por el hígado y se utiliza en la gluconeogénesis o para la obtención de energía. Cuando se producen incrementos considerables de las cifras de lactato sérico con disminución del metabolismo de conversión de lactato a piruvato se instala un cuadro de acidosis metabólica a menudo grave que puede llevar a la persona a la muerte, el rango de aparición de esta acidosis láctica depende del nivel de adaptación de cada atleta.
Se ha señalado la existencia de síntomas, a menudo solapados, que preceden al cuadro de acidosis, como son náuseas, anorexia, vómitos, diarreas, sed, dolor epigástrico. Posteriormente, puede aparecer toma de conciencia que puede ser progresiva hasta llegar al coma, acompañando a síntomas de deshidratación, hipotensión arterial que puede llegar al shock, etcétera.
Efectos fisiológicos provocados por la acidemia
- Cardiovasculares: sobre todo si el pH se encuentra entre 7.1 y 7.15, ocurre el empeoramiento de la contractilidad miocárdica, dilatación arteriolar con venocontricción, aumento de la resistencia vascular pulmonar, hipotensión, disminución del umbral para arritmias ventriculares, potencialmente fatales, disminución de la respuesta cardíaca a las Catecolaminas.
- Respiratorios: Hiperventilación, fatigabilidad muscular, disnea.
- Metabólicos: Resistencia a la insulina, inhibición de la glucólisis anaerobia, reducción de la síntesis de ATP, hiperpotasemia (sube a 0,6 mEq/L por cada 0,10 unidades que disminuya el pH). Los cambios en las concentraciones de electrolitos en el interior de las células musculares producidos por una contracción intensa se pueden resumir en un descenso del potasio (6-20 %) y fosfocreatina (70-100%), y un incremento del lactato (+ 10%), sodio (2%) y pequeños incrementos de cloro (McKenna, 1992). Estos cambios ejercen un importante efecto en la función muscular y contribuyen al desarrollo de la fatiga muscular. El efluvio de potasio desde los músculos esqueléticos que se contraen, debe, consecuentemente elevar su concentración intersticial y reducir la intracelular. Esto repercute en la despolarización del sarcolema y de los túbulos T de las membranas, con la consecuente fatiga (McKenna, 1992). Los niveles de ácido láctico intra y extracelular aumentan en función de la duración del ejercicio de alta intensidad (Osnes y Hermansen, 1976) Igualmente, se ha establecido una correlación entre los niveles de hidrogeniones en músculo y un descenso de la fatiga muscular (Costill y otros, 1988). Además, la recuperación está relacionada con una rápida renovación del lactato y de los hidrogeniones desde las células musculares (Costill y cols., 1988). Concretamente, la troponina (proteína miofibrilar) que bombea el calcio es inhibida por el descenso del pH, imposibilitando la formación del complejo actomiosina que es el responsable de generar tensión en los músculos (Fuchs y cols., 1969), al no poder liberar calcio del retículo sarcoplásmico (Nakamura y Schwartz, 1970).
- Cerebrales: obnubilación y coma.
Nota: La mayoría de las acidosis metabólicas son agudas; sin embargo, la insuficiencia renal y la acidosis tubular renal pueden asociarse con acidosis crónica; en estas condiciones, parte de la amortiguación del H+ retenido se lleva a cabo con el carbonato proveniente del hueso. Cuando esta alteración ocurre en niños, retarda el crecimiento y produce raquitismo; en los adultos, da lugar a osteítis fibrosa quística y osteomalacia.
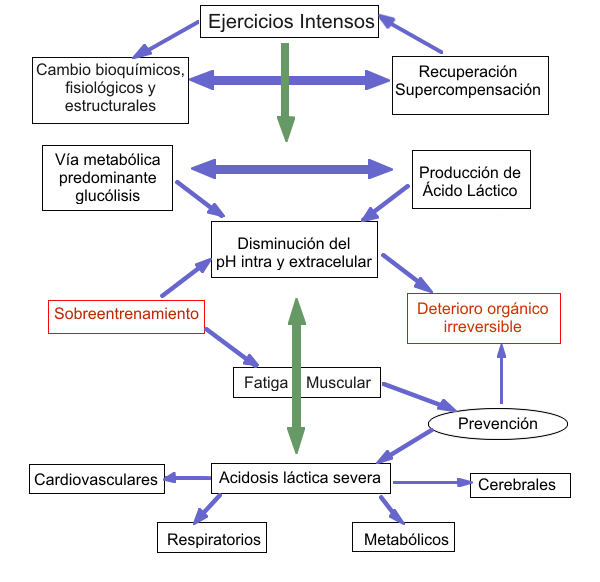
Es importante concebir, por tanto, a la fatiga como un mecanismo de defensa que se activa ante el deterioro de determinadas funciones orgánicas y celulares (cambios metabólicos, hipoxia, alteraciones hidroelectrolíticas, alteraciones térmicas, disminución de sustratos metabólicos, etc.), previniendo la aparición de lesiones celulares irreversibles y numerosas lesiones deportivas, además de prevenir los efectos de una acidosis láctica severa.
Figura 1. Esquema la fatiga como mecanismo de defensa.
CONCLUSIONES
Sabemos que “entrenar, es entrenar una reacción enzimática”. Cuando aplicamos una carga de entrenamiento la interrupción de la homeostasis estará determinada por un aumento de los procesos catabólicos o degenerativos, éstos se mantendrán hasta que dure la influencia de la carga de trabajo, casi de forma inmediata el organismo responderá a la agresión con un aumento de los procesos generativos o anabólicos (lo que llamamos recuperación) a fin de dar protección al organismo por las pérdidas energéticas sufridas ante el esfuerzo realizado por la carga de entrenamiento.
Podemos concluir entonces que si realizamos ejercicios de intensidad máxima estamos expuestos a un mayor rango de pérdida del equilibrio del organismo, sobre todo nuestro equilibrio ácido-base. La pérdida de este balance como hemos analizado en nuestro artículo puede traer consigo el establecimiento de una acidosis láctica, cuyos efectos nocivos al organismo son variados.
Además, puede concluirse que la fatiga, definida como la imposibilidad de generar una fuerza, requerida o esperada, se comporta como una base del fenómeno de adaptación encaminada a evitar lesiones irreversibles y aunque la fatiga es un concepto asociado a rendimientos inferiores a los que potencialmente es capaz de realizar un atleta, o a mecanismos de defensa que se activan ante el deterioro de determinadas funciones orgánicas y celulares, no se debe olvidar que en el entrenamiento deportivo la fatiga es un estado imprescindible para poder conseguir respuestas de adaptación, siempre que ésta se ordene de forma que no conduzca a estados de sobreentrenamiento, pues puede llegar a ser (el sobreentrenamiento) la causa de una acidosis láctica instalada con graves consecuencias.
Siempre que se entrene con el objetivo de lograr una supercompensación en el atleta, no existen procedimientos específicos de tratamiento, con fármacos o algo así, propiamente dicho para eliminar esta condición, si bien, la adopción de medidas protectoras, como por ejemplo, un buen entrenamiento o acondicionamiento físico, u otras estrategias de ayuda ergogénica que pueden retardar su aparición o disminuir su duración. La suplementación oral con álcalis es un tema sujeto a debate debido a que si bien puede retrasar la fatiga muscular por concepto de eliminar mayor concentración de iones H+, puede llegar a establecer en el atleta un estado de alcalosis, cuyos efectos también son nocivos para el organismo humano.
REFERENCIAS
1. Volkov, N.I. y Mensikov, V.V (1990). Bioquímica. No Disponible. Moscú
2. Sergeyevich M. V. y Dmitriyevich M. V (1990). Fisiología del deportista. No Disponible. España
3. Legido, J.C (1986). Fatiga y entrenamiento. III Jornadas Nacionales de Medicina en Atletismo. Pamplona. ANAMEDE, pp.: 109-120
4. No Disponible (1990). Compendio de Fisiología para Ciencias de la Salud. No Disponible
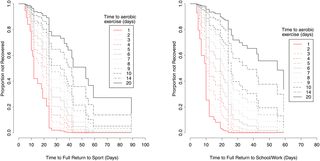
Un horario más temprano de ejercicio aeróbico se asocia con una recuperación más rápida tras una conmoción cerebral deportiva aguda
Ejercicio aeróbico y recuperación tras una conmoción: ¿Cuándo iniciar? La reciente investigación...

La nutrición de precisión debe considerar la rentabilidad para ofrecer beneficios a los pacientes
Nutrition de Precisión y Costo-efectividad: Un Enfoque Esencial para los Nutricionistas La...
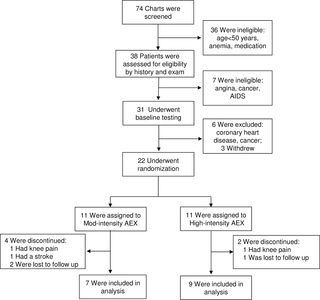
Un ensayo aleatorizado de ejercicios aeróbicos en hombres mayores infectados por el VIH: Perspectivas sobre estrategias para un envejecimiento exitoso con el VIH
Ejercicio Aeróbico en Hombres Mayores Infectados por VIH: Un Camino hacia el Envejecimiento...
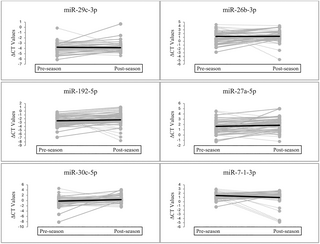
Estabilidad de las medidas de microARN salival a lo largo de una temporada de fútbol de la División I de la NCAA: Implicaciones del microARN como biomarcador de conmoción cerebral
En un esfuerzo por mejorar la gestión de conmociones cerebrales en deportistas, un estudio...

La aclimatación al calor mejora el rendimiento en el ejercicio
Resumen Este estudio examinó el impacto de la aclimatación al calor en la mejora del rendimiento...