¿Por qué los hombres acumulan grasa visceral abdominal?
Publicado 26 de enero de 2020, 11:39
Los mecanismos subyacentes de por qué los hombres son más propensos que las mujeres a acumular grasa visceral abdominal siguen sin estar claros. La evidencia indica que una vez que el intestino absorbe la grasa de la dieta, las lipoproteínas intestinales producidas entre hombres y mujeres no son idénticas.
La acumulación de grasa es el resultado de una mayor ingesta de calorías en relación con el gasto de energía. Desde la perspectiva de los adipocitos, esto corresponde a una mayor absorción de nutrientes desde la descomposición de la grasa. El catabolismo graso de los adipocitos, también conocido como lipólisis, está mediado en parte por la epinefrina. Al unirse la epinefrina a los receptores adrenérgicos β, se estimula la lipólisis. Esta acumulación de grasa visceral abdominal en los hombres, es un fuerte predictor independiente de mortalidad, y se debe principalmente a la mayor absorción de grasa en la dieta por su grasa visceral abdominal. Dado que la grasa de la dieta es absorbida por los enterocitos y transportada a la circulación en forma de quilomicrones y lipoproteínas de muy baja densidad (VLDL), es crucial entender cómo estas lipoproteínas son diferentes entre hombres y mujeres.
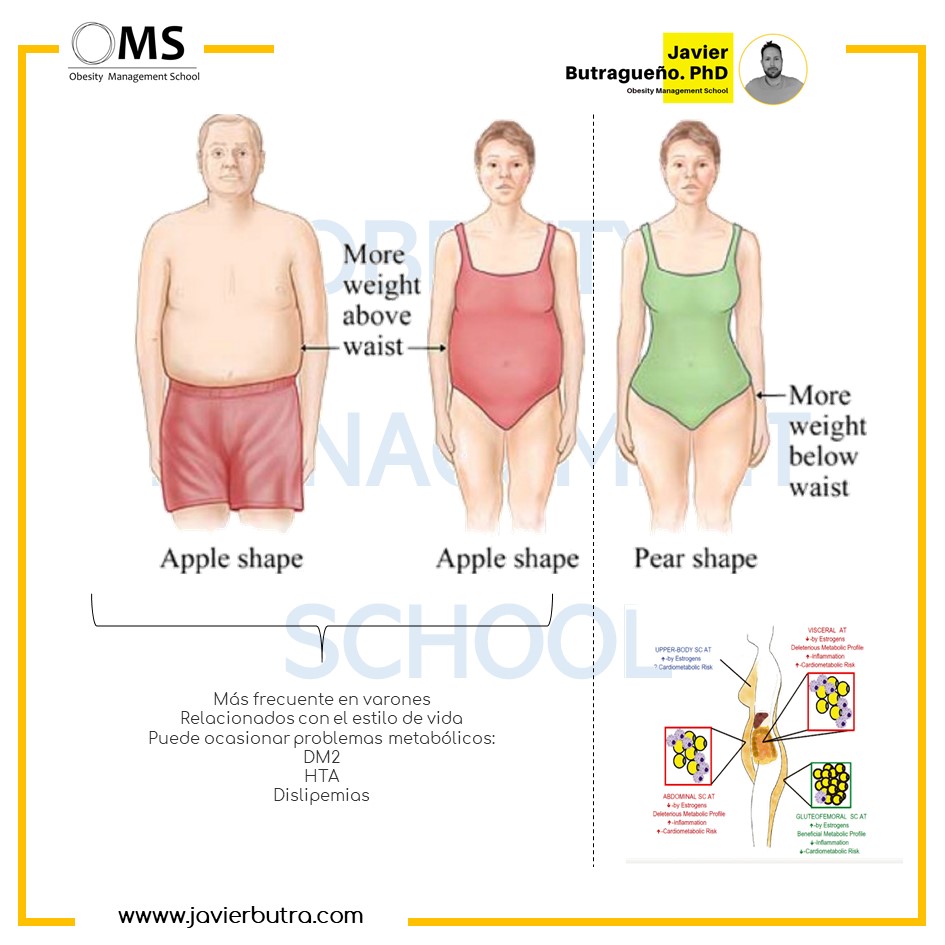
Los quilomicrones* en los hombres son generalmente de mayor tamaño y con una mayor cantidad que los de las mujeres.
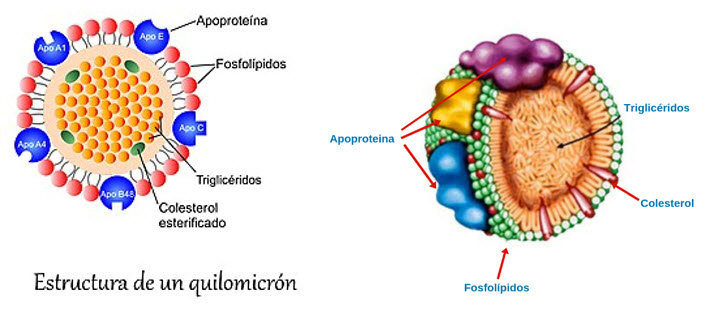 |
| Los quilomicrones son lipoproteínas que tienen la función de transportar los lípidos procedentes de la dieta hasta el hígado y otros tejidos. Se sintetizan en las células de la pared intestinal desde donde pasan al plasma sanguíneo. Son el tipo de lipoproteína de mayor tamaño, superando los 100 nm |
Durante el estado posprandial, estos quilomicrones congestionan la lámina propia y los linfáticos de baja presión. Los ácidos grasos liberados luego son almacenados por los adipocitos viscerales abdominales cercanos, lo que lleva a la acumulación de grasa visceral abdominal. Estos mecanismos quizás explican por qué los hombres, a través de su mayor producción de quilomicrones, tienen más probabilidades de acumular grasa visceral abdominal que las mujeres. Esta acumulación eventualmente conduce al aumento del abdomen, lo que confiere a los hombres su cuerpo en forma de manzana.
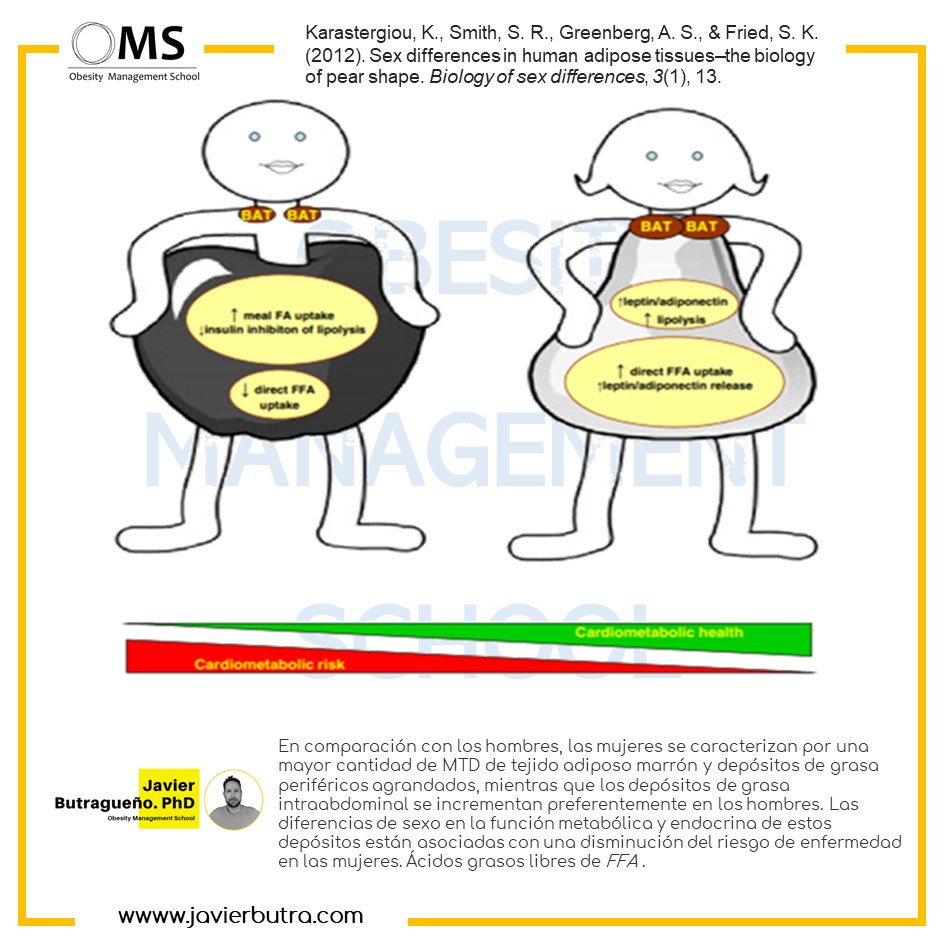
La acumulación excesiva de grasa visceral abdominal también se conoce como obesidad androide. Por otro lado, la forma de pera a menudo se atribuye a las mujeres debido a su tendencia a acumular grasa subcutánea en las regiones del muslo (femoral) y glúteo, que también se conoce como obesidad ginoidea.
Los estudios han demostrado que el estrógeno reduce la lipólisis en los adipocitos subcutáneos de los glúteos. La reducción de la lipólisis en los adipocitos subcutáneos de los glúteos en las mujeres probablemente se deba al aumento mediado por el receptor de estrógenos en los receptores α2A. Sin embargo, la acumulación neta de grasa en un depósito de grasa particular depende no solo de su lipólisis de adipocitos sino también de la absorción de nutrientes de sus adipocitos, así como de su número total de adipocitos.
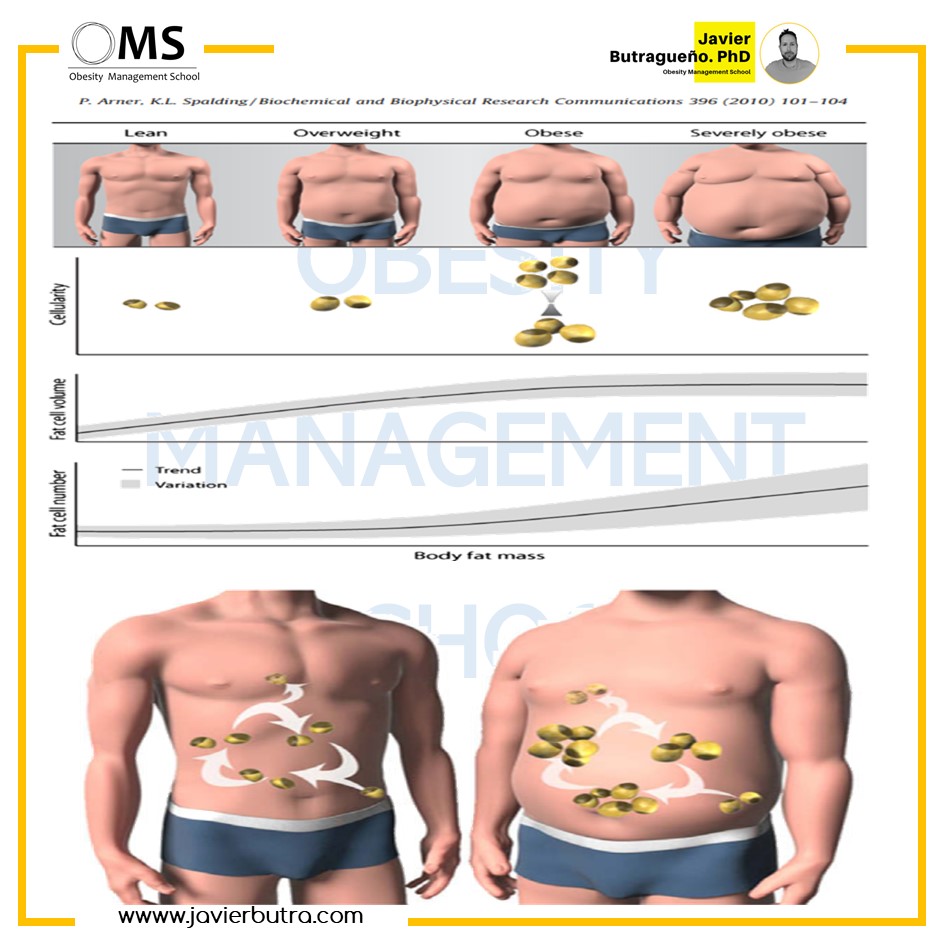
Dado que el estrógeno es capaz de estimular la proliferación preadipocítica humana, la reducción de la lipólisis subcutánea de los glúteos no necesariamente puede conducir a una reducción general en la lipólisis del depósito de grasa subcutánea de los glúteos. De hecho, los estudios que comparan la lipólisis y la absorción de nutrientes de varios depósitos de grasa indican que las mujeres tienen más lipólisis que los hombres en el depósito de grasa de la parte inferior del cuerpo, mientras que los hombres tienen más lipólisis que las mujeres en el depósito de grasa visceral abdominal. En otras palabras, las mujeres acumulan más grasa en el depósito subcutáneo principalmente porque ese depósito absorbe más grasa. Del mismo modo, los hombres acumulan más grasa en el depósito visceral abdominal porque su depósito de grasa absorbe más grasa que las mujeres.
Grasa corporal
Las diferencias de sexo en la composición corporal están bien establecidas según diferentes autores. Para el mismo índice de masa corporal (IMC), las mujeres generalmente presentan ~ 10% más de grasa corporal en comparación con los hombres. Es importante destacar que las diferencias entre los dos sexos no solo están en el porcentaje de grasa corporal total sino también en su distribución a las diferentes partes del cuerpo.
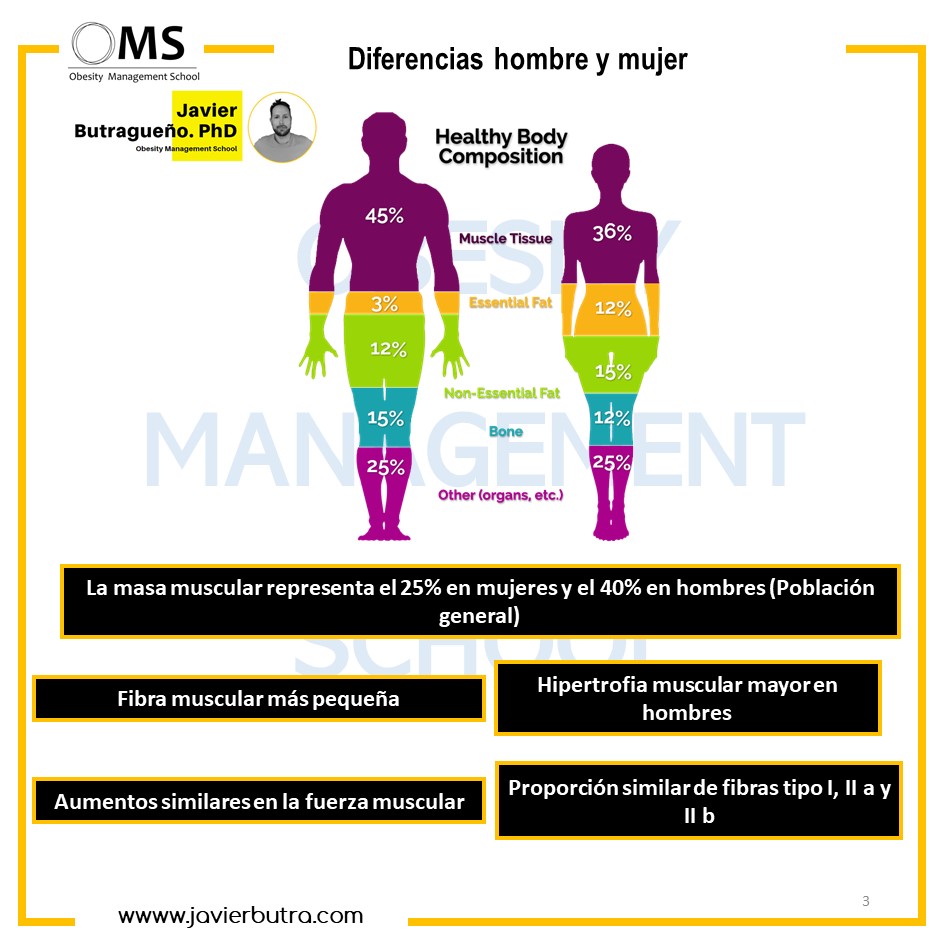
El envejecimiento aumenta la adiposidad en ambos sexos, pero nuevamente, las mujeres se caracterizan por un mayor porcentaje de grasa corporal a lo largo de toda la vida.
A niveles comparables de adiposidad total (estimado a partir del IMC o mediante técnicas de imagen), las mujeres tienen más SAT tanto en el abdomen como en el área gluteofemoral.
Las diferencias sexuales notables surgen durante la pubertad: el aumento del peso corporal en los niños se debe principalmente al aumento de la masa magra, mientras que en las niñas debido al aumento de la masa grasa; Las distribuciones típicas de grasa androide y ginoidea también aparecen por primera vez durante este período.
La menopausia es seguida por la redistribución del tejido adiposo hacia un fenotipo más central / androide. Es importante destacar que es la adiposidad visceral que aumenta en las mujeres durante la transición perimenopáusica, presumiblemente debido a la caída en los niveles de estrógenos. A medida que la testosterona disminuye con la edad, la adiposidad visceral también aumenta en los hombres.
Tipos de grasa corporal
La grasa corporal se puede clasificar en grasa marrón, beige y blanca según autores como Harms y Seale. En términos de abundancia relativa en las mitocondrias, la grasa marrón es la más abundante y la grasa blanca es la menos. A diferencia de la grasa marrón y beige, la grasa blanca no es capaz de realizar termogénesis. La grasa corporal en humanos adultos se compone principalmente de grasa blanca.
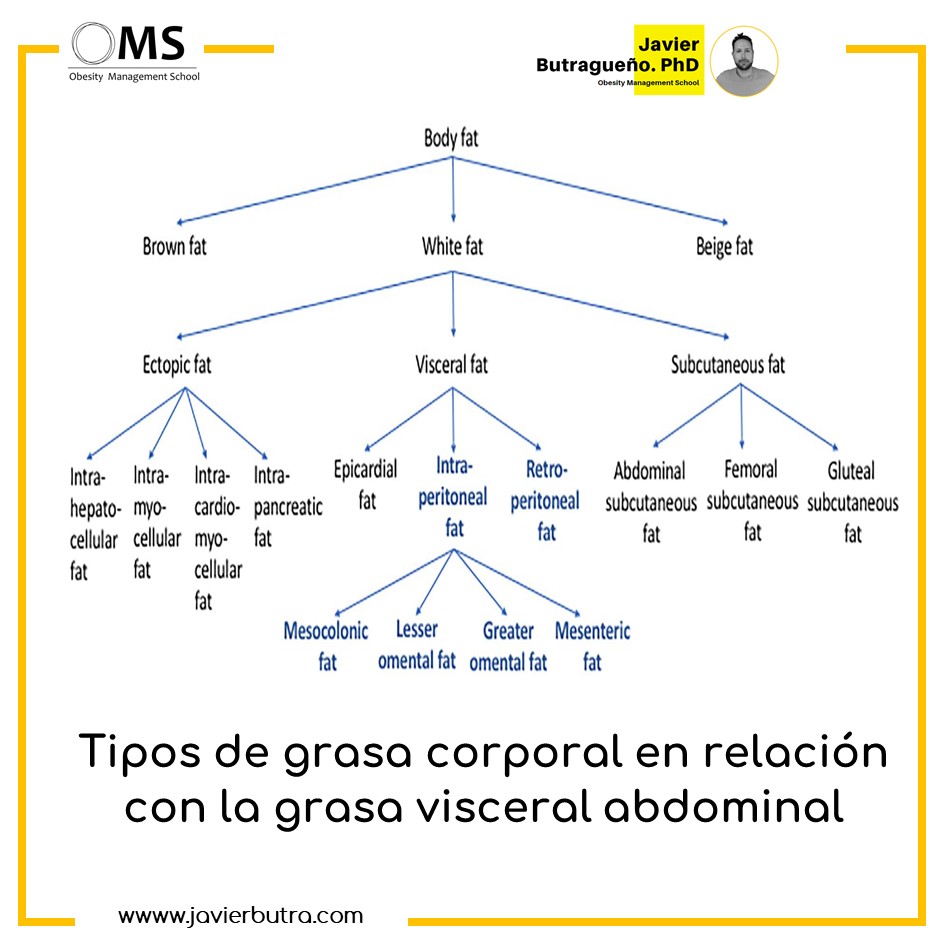
Según su ubicación en el cuerpo, la grasa blanca puede subcategorizarse en grasa subcutánea, visceral y ectópica. La grasa ectópica, que es la menor en cantidad, se encuentra dentro de los órganos internos. La grasa intrahepatocelular, la grasa intrapancreática, la grasa intramiocelular y la grasa intracardiomiocelular se consideran grasas ectópicas.
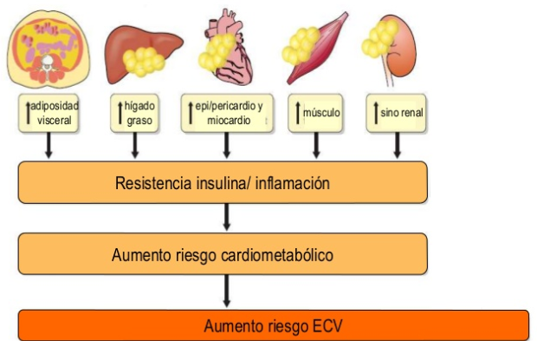
La grasa que rodea los órganos internos generalmente se considera grasa visceral. La grasa epicárdica y la grasa visceral abdominal rodean la miocardia y los órganos gastrointestinales, respectivamente, y ambas se consideran grasa visceral.
La grasa subcutánea, que es más abundante en las mujeres, se encuentra en toda la capa profunda de la piel (hipodermis). Los depósitos de tejido adiposo blanco subcutáneo (SAT), justo debajo de la piel, almacenan ~ 80-90% de la grasa corporal total, principalmente en las áreas abdominal (alrededor de la cintura), subescapular (en la parte superior de la espalda), glúteo y femoral (muslo). Estos tejidos adiposos subcutáneos tienen distintos perfiles morfológicos y metabólicos y exhiben diferencias de tamaño y función específicas del sexo.
A medida que se acumula grasa visceral en el abdomen, el vientre se vuelve visiblemente más grande, un fenómeno que comúnmente se conoce como desarrollo de grasa abdominal. Hay que destacar que la grasa del abdomen consiste no solo en grasa visceral abdominal sino también en grasa subcutánea abdominal. Aunque la circunferencia de la cintura se correlaciona fuertemente con la grasa abdominal total, no se correlaciona tanto con la grasa visceral abdominal. Además, la correlación de la circunferencia de la cintura con la grasa visceral abdominal es más débil en las mujeres que en los hombres. Por lo tanto, la inferencia de la cantidad de grasa visceral abdominal de la circunferencia de la cintura debe hacerse con precaución, especialmente en las mujeres.
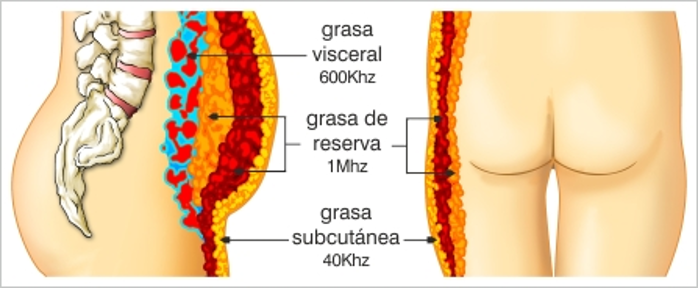
Los depósitos intraabdominales incluyen tejidos adiposos viscerales (VAT, omental and mesenteric) que están asociados con los órganos digestivos. El VAT drena su sangre en la vena porta y representa el 6-20% de la grasa corporal total, con valores más altos en hombres que en mujeres. Los tejidos adiposos en el compartimento retroperitoneal (~ 7% del total) no drenan en la vena porta y, por lo tanto, no se consideran "viscerales".
Grasa visceral abdominal
Para comprender la grasa visceral abdominal, se justifica una mirada más cercana a la anatomía de los mesenterios y el retroperitoneo. Los mesenterios conectan los órganos gastrointestinales que se encuentran dentro de la cavidad abdominal con la pared de la cavidad abdominal. La mayoría de las conexiones se realizan a la pared posterior en lugar de la anterior de la cavidad abdominal. Como tal, los órganos que residen dentro de la pared posterior de la cavidad abdominal no tienen mesenterios. Estos órganos se conocen comúnmente como órganos retroperitoneales. Los dos órganos retroperitoneales son páncreas y duodeno. La grasa que rodea estos órganos retroperitoneales se conoce como grasa retroperitoneal. Hay que tener en cuenta que otros órganos retroperitoneales, como los riñones o el colon, no se muestran en la imagen.
Tanto la grasa intraperitoneal como la grasa retroperitoneal constituyen grasa visceral abdominal, lo que explica por qué muchos investigadores incluyen la grasa retroperitoneal al medir la grasa visceral abdominal. Hay varias razones para considerar la grasa retroperitoneal como parte de la grasa visceral abdominal. Primero, la grasa retroperitoneal rodea los órganos retroperitoneales. Por lo tanto, debe clasificarse como visceral en lugar de grasa ectópica o subcutánea. En segundo lugar, el líquido linfático del tracto gastrointestinal drena a través de los vasos linfáticos más pequeños dentro de los mesenterios antes de ingresar a los vasos linfáticos más grandes. Tercero, a diferencia de la grasa subcutánea, tanto la grasa retroperitoneal como la intraperitoneal aumentan el riesgo de síndrome metabólico. Por lo tanto, es concebible que la grasa visceral abdominal incluya grasa tanto intraperitoneal como retroperitoneal.
El hecho de que la grasa visceral abdominal a menudo se denomina simplemente "grasa visceral" a veces puede causar confusión. Cuando se mide la cantidad de “grasa visceral” desde la región abdominal, podría decirse que es más apropiado etiquetarla como grasa visceral abdominal en lugar de “grasa visceral”. Como se mencionó anteriormente, la grasa visceral incluye no solo la grasa visceral abdominal sino también depósitos de grasa que rodean otros órganos no abdominales, como la grasa epicárdica.
La grasa visceral abdominal está fuertemente asociada con anormalidades metabólicas
Aunque la grasa subcutánea abdominal y la grasa intrahepatocelular están asociadas con un mayor riesgo de mortalidad en los hombres, solo la grasa visceral abdominal es un fuerte predictor independiente de mortalidad en los hombres. La asociación de la grasa visceral abdominal con la mortalidad no es exclusiva de los hombres, ya que también es un fuerte predictor de mortalidad en mujeres con obesidad. En consecuencia, es importante comprender la patogenia de la grasa visceral abdominal y su asociación con complicaciones metabólicas.
La obesidad puede impedir las funciones de la microvasculatura. Los estudios en ratones machos han revelado que la obesidad androide está asociada no solo con la resistencia a la insulina sino también con una disminución de la densidad capilar y un aumento de la permeabilidad macromolecular. Esta disfunción microvascular eventualmente puede conducir al desarrollo de hipertensión, que es uno de los criterios del síndrome metabólico. El aumento de la permeabilidad vascular en la obesidad androide también sugiere que la acumulación de grasa en el depósito visceral abdominal es causada por la desregulación de las células endoteliales vasculares. En este sentido, las células endoteliales que recubren las vasculaturas afectadas pueden ser un contribuyente clave en el desarrollo de la obesidad androide como se sugiere en una hipótesis de comunicación bidireccional propuesta recientemente sobre la disfunción vascular en la obesidad
Graupera, M., & Claret, M. (2018). Endothelial cells: new players in obesity and related metabolic disorders. Trends in Endocrinology & Metabolism, 29(11), 781-794.
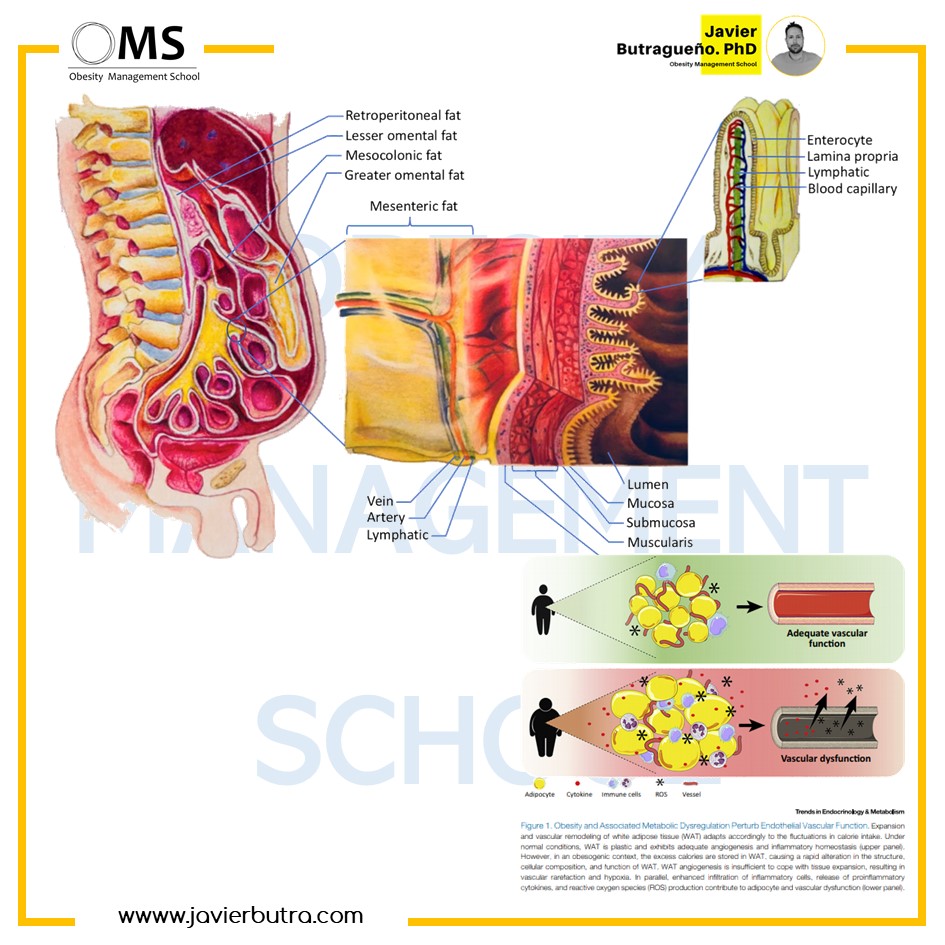
A medida que se acumula la grasa visceral abdominal, aumenta la infiltración de macrófagos. Se sabe que los macrófagos infiltrados liberan citocinas inflamatorias. Estas citocinas, que incluyen TNFα, son capaces de hacer que los adipocitos viscerales abdominales circundantes se vuelvan resistentes a la insulina y liberen sus ácidos grasos. Este flujo de ácidos grasos es perjudicial para el hígado y el páncreas.
El órgano que posiblemente segrega la mayor cantidad de grasa es el intestino delgado, particularmente durante el estado posprandial. El intestino, está rodeado por la grasa visceral abdominal. Por lo tanto, no es sorprendente que la grasa visceral abdominal pueda absorber una cantidad bastante significativa de grasa dietética de las lipoproteínas intestinales. Los estudios han demostrado que aproximadamente el 21% de la grasa ingerida se almacena en la grasa intraperitoneal y aproximadamente el 6% de la misma se almacena en la grasa retroperitoneal por los hombres. En contraste, solo alrededor del 5% de la grasa ingerida es almacenada en la grasa intraperitoneal por las mujeres.
Para comprender mejor por qué la grasa visceral abdominal de los hombres absorbe más grasa de la dieta que la de las mujeres, es necesario un análisis más detallado del proceso de absorción de grasa en la dieta. La grasa de la dieta es digerida y absorbida por el intestino delgado. La grasa dietética absorbida es secretada por los enterocitos en dos formas principales: quilomicrones (> 80 nm de diámetro) y VLDL (30–80 nm).
Es importante destacar que cuando el intestino delgado es desafiado con una mayor cantidad de grasa, producirá quilomicrones más grandes. Estos quilomicrones más grandes tienden a acumularse en la mucosa intestinal, dado que los hombres generalmente consumen una mayor cantidad de grasa en la dieta debido a su mayor ingesta, y se espera que produzcan quilomicrones más grandes y más que las mujeres.
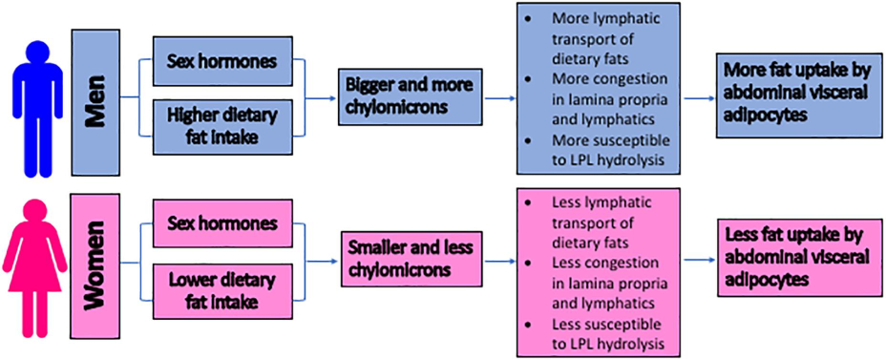
Why Do Men Accumulate Abdominal Visceral Fat? Andromeda M. Nauli, Sahar Matin. Frontiers in Physiology, 10, 12 2019
De todos los factores que contribuyen a la acumulación de grasa visceral abdominal, el estilo de vida es posiblemente el más importante.
Según los autores del estudio, distribuir la cantidad de ingesta de grasas en la dieta en varias comidas más pequeñas debería reducir la probabilidad de acumulación de grasa visceral abdominal al reducir tanto el tamaño como la cantidad de quilomicrones. Reducir la carga de lípidos en el intestino delgado también será beneficioso para las funciones de los vasos linfáticos colectores, ya que la alta carga de lípidos reduce su frecuencia y amplitud de contracción. Al mantener la contracción linfática, las comidas más pequeñas pueden reducir el tiempo de retención de los quilomicrones en la lámina propia. En consecuencia, esto reduciría la probabilidad de acumulación de grasa visceral abdominal.
Aunque nuestra visión es algo diferente a la de los autores, es interesante tener presente este trabajo para individualizar en algunos contextos específicos.
Otro aspecto importante del estilo de vida es el ejercicio. Además de aumentar el gasto de energía, el ejercicio puede ralentizar la acumulación de grasa visceral abdominal al aumentar el flujo de los quilomicrones dentro de la lámina propia y los vasos linfáticos, así como reducir tanto la expresión de LPL en la grasa mesentérica como la filtración de los linfáticos.
Hay otros factores potenciales que pueden contribuir al desarrollo de la grasa visceral abdominal. Según los mecanismos propuestos por los autores, hacer ejercicio y comer una dieta baja en grasas, o al menos distribuir la ingesta de grasas en varias comidas más pequeñas, debería ayudar a ralentizar el desarrollo de la grasa visceral abdominal.
REFERENCIAS REVISADAS
Why Do Men Accumulate Abdominal Visceral Fat? Andromeda M. Nauli, Sahar Matin. Frontiers in Physiology, 10, 12 2019
Schorr, M., Dichtel, L. E., Gerweck, A. V., Valera, R. D., Torriani, M., Miller, K. K., & Bredella, M. A. (2018). Sex differences in body composition and association with cardiometabolic risk. Biology of sex differences, 9(1), 28.
Samuel, V. T., & Shulman, G. I. (2016). The pathogenesis of insulin resistance: integrating signaling pathways and substrate flux. The Journal of clinical investigation, 126(1), 12-22.
Karastergiou, K., Smith, S. R., Greenberg, A. S., & Fried, S. K. (2012). Sex differences in human adipose tissues–the biology of pear shape. Biology of sex differences, 3(1), 13.
