Los efectos moduladores del entrenamiento con ejercicios sobre las disfunciones inmunometabólicas inducidas por la obesidad
Publicado 7 de mayo de 2020, 14:15
Recientemente dos campos han cogido fuerza dentro del entendimiento de la obesidad. El metabolismo y la inmunología , conocido como inmunometabolismo. Es importante entender que estos dos términos vinculan el estado metabólico con la inflamación sistémica. Descubrir la producción del factor de necrosis tumoral α (TNFα) en el tejido adiposo (AT) fue el primer paso para desarrollar el campo del inmunometabolismo. Luego, descubriendo la infiltración de macrófagos (MФ) en el tejido adiposo blanco (WAT) arroja nuevas ideas sobre este campo.
El tejido adiposo actúa como un sensor del estado metabólico y un activador de los órganos endocrinos, debido en parte a la secreción de más de 50 factores bioactivos llamados adipocinas.
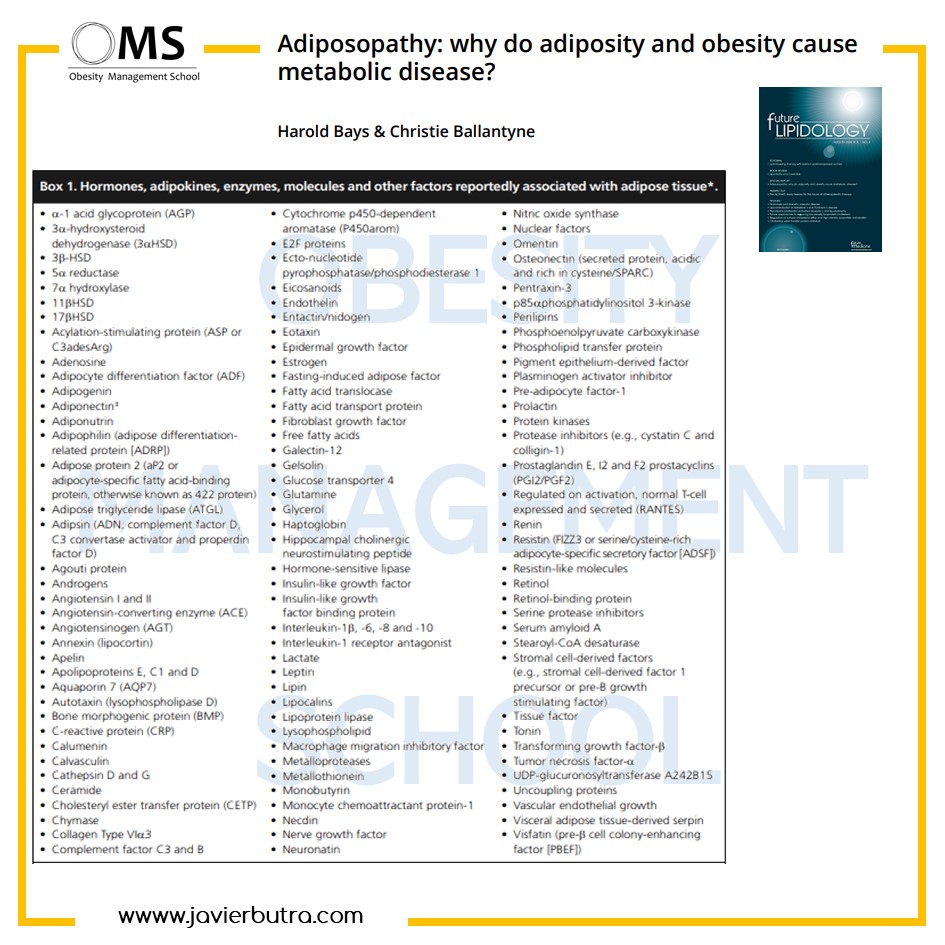
El mantenimiento de la homeostasis del AT se maneja mediante una interacción entre el sistema inmunitario, el estroma (fibroblastos, precursores de adipocitos, células endoteliales y del músculo liso endotelial) y las células parenquimatosas, denominadas función vascular estromal (SVF). En consecuencia, el sistema inmunitario preserva la homeostasis mediante la inhibición de la inflamación y el control de la remodelación de AT.
Un estilo de vida desequilibrado conduce al almacenamiento del exceso de calorías en los adipocitos, la hipertrofia y la expansión de WAT que induce la limitación del espacio extracelular y espacios de micro hipoxia. Después de estos cambios morfológicos, los adipocitos y el SVF promueven la expresión de factores de estrés que inducen el deterioro de la homeostasis que causa el desarrollo de una inflamación sistémica crónica de bajo grado y metainflamación.
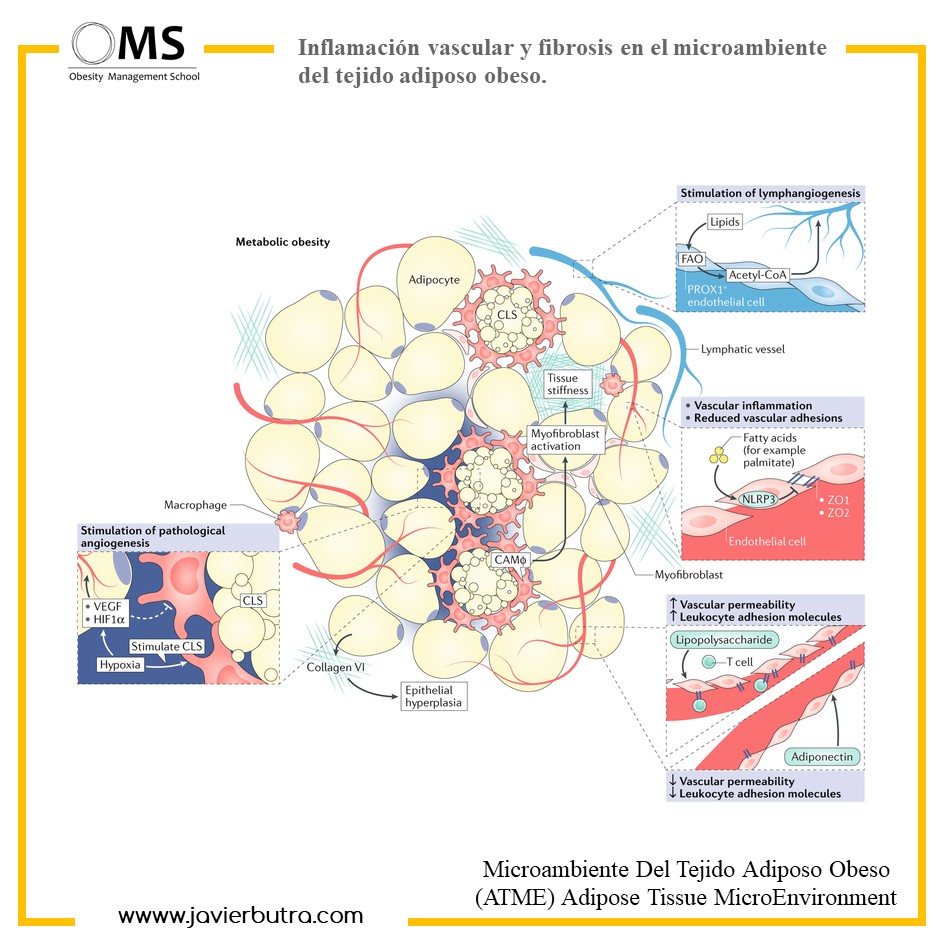
La metainflamación es diferente de una inflamación típica debido al tipo de activadores, la ubicación de las células inmunes reclutadas y la duración y / o intensidad de las actividades del sistema inmunitario durante un estado inflamatorio. Una inflamación aguda ha sido promovida por patógenos exógenos invasivos que conducen a la estimulación del sistema inmune que induce una inflamación local de alta intensidad a corto plazo. Por el contrario, se ha desarrollado una metainflamación por el exceso de nutrientes, estimulantes endógenos, que provoca la provocación del sistema inmunitario y promueve una inflamación sistémica crónica de bajo grado.
En los últimos años, debido al descubrimiento de los niveles basales más bajos de células inflamatorias y citocinas entre individuos físicamente activos, la terapia con ejercicios se ha prescrito con frecuencia como un enfoque práctico no invasivo para el tratamiento de enfermedades metabólicas. El entrenamiento, promueve varios mecanismos antiinflamatorios que conducen a mejoras en el estado metabólico y los perfiles inflamatorios.
El papel del sistema inmune en la homeostasis del tejido adiposo
En los últimos años, se ha desarrollado una revolución científica al revelar una fuerte asociación entre los sensores de nutrientes y las señales inmunes. Los diferentes tipos de células inmunes acumuladas en el tejido adiposo magro inducen respuestas inmunes tipo 2 para inhibir las vías inflamatorias y mantener la homeostasis del tejido. Esto se caracteriza por la acumulación de citocinas antiinflamatorias, como la interleucina (IL) -5/13/4/10. Los macrófagos M2 tienen características antiinflamatorias que generan principalmente los mediadores antiinflamatorios como IL-10. Por otro lado, la fuente principal de producción de IL-4 son los eosinófilos (EOS), y la reducción de EOS en el tejido adiposo visceral se acompaña por frecuencias disminuidas de macrófagos antiinflamatorios del tejido adiposo. Varios estudios han demostrado que este eje es un mecanismo regulador crítico en la homeostasis de AT. En este sentido, las alteraciones morfológicas del tejido adiposo inducidas por la obesidad afectan el número y el fenotipo de las células inmunes.
Una dieta alta en calorías promueve muchos cambios en AT que inducen la remodelación de AT. Los estudios han demostrado que estos cambios conducen a la formación de un número significativo de estructuras en forma de corona (CLS). Estas estructuras se han demostrado como un solo adipocito muerto en tejido adiposo obeso (OAT) humano. e observa que los CLS son los personajes prominentes de la alteración de la homeostasis AT que conducen a la inflamación sistémica crónica de bajo grado. En este contexto, la clasificación de la obesidad basada en el número de trastornos del síndrome metabólico (MetS) se correlaciona con el porcentaje de CLS. Además, existe una fuerte asociación entre este tipo de estructuras y riesgo de resistencia a la Insulina, problemas cardiovasculares, pronóstico de cáncer, etc. Es importante destacar que la presencia de adipocitos muertos persiste incluso hasta 30 veces en el OAT.
Los MФs son el brazo fuerte de la inmunidad innata y realizan una amplia gama de funciones a través de la distinción de fenotipos. Debido a su polarización fenotípica en un entorno y condición patológica diferentes, pueden adoptar fenotipos funcionales distintos.En el AT, los MФs desempeñan múltiples funciones en la defensa del “huésped” (a través de la formación y eliminación de una respuesta inflamatoria), el desarrollo de tejidos, la monitorización de las alternancias de estos tejidos (mediante la detección de moléculas invasoras con sus diversos sensores) y, en particular, en el mantenimiento de la homeostasis de los tejidos (cambios de estructura y maduración, remodelación apoptótica y reparación de células y / o tejidos). El ciclo de muerte celular y reemplazo de adipocitos ocurre regularmente, en este caso, los MФs del tejido adiposos tienen un papel fundamental en estos procesos. En otras palabras, tienen una capacidad considerable tanto para eliminar los adipocitos muertos como para inhibir la formación de CLS en la homeostasis del AT.
También se ha comprobado que desempeñan un papel importante durante las funciones metabólicas agudas. Un rápido reclutamiento de macrófagos del tejido adiposo se revela durante la lipólisis. Estas células adquieren un fenotipo inflamatorio y comienzan a amortiguar los lípidos para supervisar el gradiente liberado a la circulación gradualmente para recolectar y depositar el exceso de ácidos grasos. Los macrófagos del tejido adiposo se han visto sobreexpresados en personas con obesidad, en esta situación, la interacción integrada entre los adipocitos y MФs de CLSs lleva a generar y mantener la inflamación crónica de bajo grado. Es decir, teniendo en cuenta las características histológicas, la inflamación de bajo grado se ha determinado por un aumento en las células inmunes, principalmente MФs. Si esta inflamación crónica de bajo grado se mantiene en el tiempo existe un aumento existe un aumento en las citocinas inflamatorias que conduce al reclutamiento, infiltración, diferenciación y activación de un mayor número de células inmunes en un ciclo difícilmente de parar. Cabe destacar, que aunque la infiltración de células inmunes siempre induce los factores inflamatorios en OAT, el fenotipo de los leucocitos reclutados puede influir en la polaridad MФ.
Entrenamiento físico como una intervención terapéutica en trastornos inmunometabólicos inducidos por la obesidad
El cambio mundial en los estilos de vida, es decir una combinación de ser sedentario, consumir nutrientes con alto contenido calórico y gestionar de manera inadecuada las emociones, ha acelerado la #obesidad. Un estilo de vida inactivo explica muchos componentes de la obesidad y trastornos metabólicos. De hecho, las enfermedades crónicas son los principales “asesinos” en la era moderna, y la inactividad física es una de las causas principales de la mayoría de estas enfermedades.
Esta inactividad física, acompañada de el exceso de nutrientes desempeña un papel fundamental en el estado metabólico, que promueven la activación crónica de las vías inflamatorias que conducen a trastornos inmunometabólicos. Parece que el entrenamiento físico induce el uso de calorías acompañado de una mejora de la salud metabólica y del estado inflamatorio. Las mioquinas producidas a través del entrenamiento físico probablemente interfieran con las vías inflamatorias. Por ejemplo, la irisina, una adipomioquina y mediador del ejercicio, se correlaciona con la condición metabólica. Estos efectos positivos del ejercicio podrían ser independientes de las alteraciones de la adiposidad. Además, investigaciones recientes en humanos han revelado mecanismos asociados con marcadores M2 después del ejercicio, mejora del estado quimiotáctico, las funciones leucocitarias, sensibilidad a la insulina, la reducción de marcadores inflamatorios y factores de riesgo metabólicos relacionados con la salud. En este sentido, se muestra que los impactos positivos de un protocolo voluntario de entrenamiento, están relacionados con la reducción del tamaño de adipocitos, la formación de CLS y el reclutamiento de células inmunes en el OAT.
Se ha informado por varios autores, que el estado inflamatorio y la función de la insulina mejoran la función vascular estromal incluso después de una sesión de ejercicio debido a la regulación negativa de TNFα, CCL2 e IL-1β. Además de los efectos del ejercicio sobre el estado inflamatorio de la AT, el entrenamiento físico influye mucho en la infiltración de MФ y los marcadores de polarización de M1 / M2 en la AT. Lo importante de esto, es que aunque no se pierda peso, se ha encontrado una menor expresión de marcadores inflamatorios en personas con obesidad después del ejercicio.
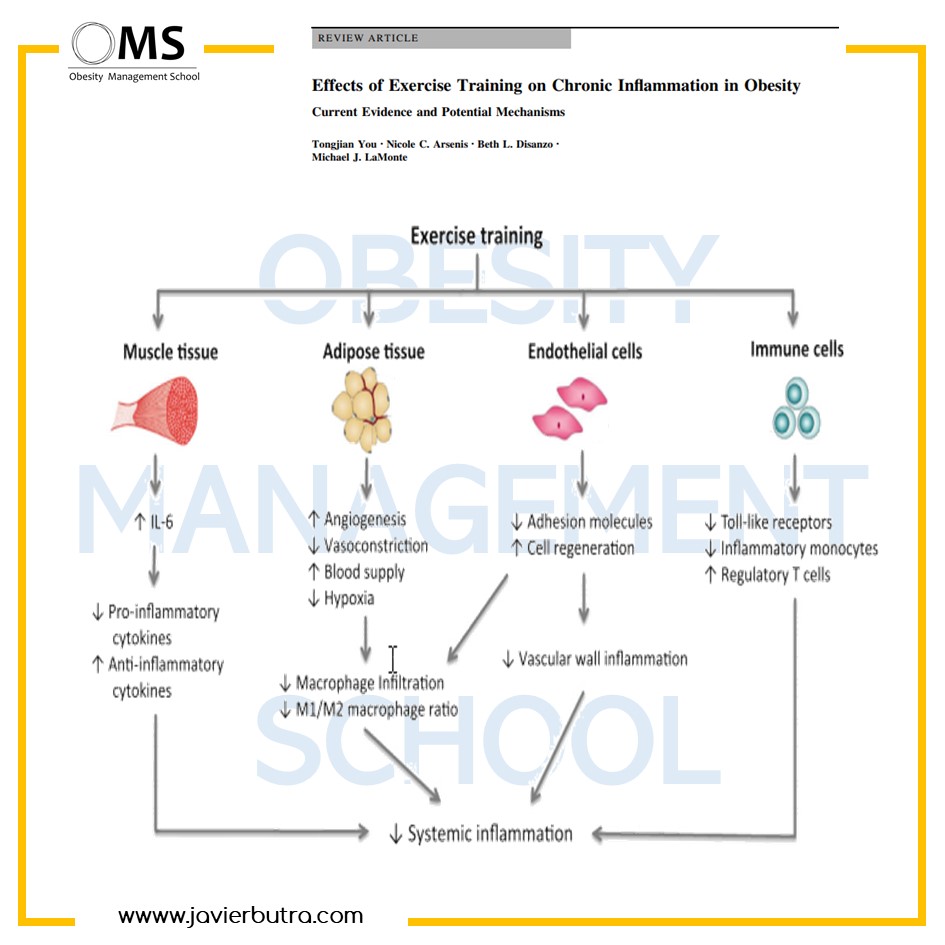
Ahora tocará saber si el mejor entrenamiento para cada persona es un HIIT, un HIFT, un entrenamiento con cargas para mejorar la potencia, la fuerza máxima o simplemente adquirir una adherencia correcta al ejercicio que nos permita mejorar y aumentar la intensidad de manera progresiva para activar diferentes vías de señalización. Lo que está cada día más claro, es que el entrenamiento físico como una estrategia no invasiva de bajo costo es ampliamente recomendado para interrumpir los mecanismos inflamatorios inducidos por la obesidad debido a su potencial para desencadenar estos mecanismos moleculares en la etapa temprana de inflamación en las células inmunes circulantes.

Referencias interesantes para consultar:
- Soltani, N., Marandi, S. M., Kazemi, M., & Esmaeil, N. (2020). The Exercise Training Modulatory Effects on the Obesity-Induced Immunometabolic Dysfunctions. Diabetes, metabolic syndrome and obesity: targets and therapy, 13, 785.
- Hotamisligil, G. S. (2017). Inflammation, metaflammation and immunometabolic disorders. Nature, 542(7640), 177.
- Castoldi, A., Naffah de Souza, C., Câmara, N. O. S., & Moraes-Vieira, P. M. (2016). The macrophage switch in obesity development. Frontiers in immunology, 6, 637.
- Wensveen, F. M., Valentić, S., Šestan, M., Turk Wensveen, T., & Polić, B. (2015). The “Big Bang” in obese fat: Events initiating obesity‐induced adipose tissue inflammation. European journal of immunology, 45(9), 2446-2456.
- Mills, C. (2012). M1 and M2 macrophages: oracles of health and disease. Critical Reviews™ in Immunology, 32(6).
- Booth, F. W., Roberts, C. K., & Laye, M. J. (2011). Lack of exercise is a major cause of chronic diseases. Comprehensive Physiology, 2(2), 1143-1211.
- Booth, F. W., Gordon, S. E., Carlson, C. J., & Hamilton, M. T. (2000). Waging war on modern chronic diseases: primary prevention through exercise biology. Journal of applied physiology, 88(2), 774-787.
