Profundizando en la Biogénesis Mitocondrial: ¿Qué hay de nuevo?
Publicado 21 de noviembre de 2018, 8:36
Laura L. Sánchez (Coordinadora Área IICEFS. Lcda. Biología. Grado Nutrición Humana y Dietética. Máster Investigación en Medicina Clínica)
Juan Ramón Heredia (Director General IICEFS. Doctorando UMH. Licdo. CCAFYD. Master Investigación Medicina Clínica)
Profundizando en la Biogénesis mitocondrial: ¿Qué hay de nuevo?
La mitocondria es uno de los orgánulos característicos de la célula eucariota con una función fundamental: Generar adenosin trifosfato (ATP). Es uno de los componentes clave del músculo esquelético y su desarrollo está muy regulado por el uso o desuso que se realiza de la propia musculatura, es decir, el contenido mitocondrial se ve ampliamente modificado tanto por ejercicio físico como por el sedentarismo.
Pero, generar energía no es su único cometido. Las mitocondrias también están relacionadas con apoptosis, generación de especies reactivas de oxígeno (ROS), mitofagia y con fenómenos de síntesis y degradación de proteínas mitocondriales, entre otros procesos metabólicos importantes.
El término “biogénesis mitocondrial” es ciertamente confuso, dado que, en realidad no se generan nuevas mitocondrias en el tejido, sino que se produce una adición de nuevas proteínas, es decir, se sintetiza nuevo contenido proteico que complementará a las mitocondrias, pudiendo verse modificada su morfología, todo con el objetivo de mejorar su funcionalidad y su eficacia energética. Así mismo, estos procesos de síntesis coexisten con otros de remodelación del contenido, antes mencionados, y que se dan a través de la fusión y la fisión de mitocondrias. Respecto a la mitofagia, es un proceso de autofagia y, por tanto, de degradación que permite eliminar aquellas mitocondrias que, por diferentes motivos, están dañadas. Las proteínas PTEN induce putative kinasa-1 (PINK1) y Parkin son parte de una de las vías más estudiadas por las que se desarrolla este proceso tan importante para el correcto funcionamiento celular(1). La fisión mitocondrial es el proceso por el cual la mitocondria se subdivide, facilitando la apoptosis de aquellos elementos dañados y, por lo general, precede a la mitofagia (2).
La mitocondria, como ya es bien conocido, posee algunos genes propios (mtDNA) que codifican, en concreto, para 13 polipéptidos relacionados con la cadena de transporte de electrones, con adición de la síntesis de otras proteínas por parte de los genes nucleares y que son necesarias para su funcionamiento. Por tanto, en la biogénesis mitocondrial se produce la regulación de ambos genomas, el nuclear y el mitocondrial, siendo relevante un buen funcionamiento de la comunicación entre ambos, por medio de determinados elementos celulares específicos de esta situación. Por ello, además de esta comunicación, es de suma importancia que los procesos por los cuales se importan las proteínas sintetizadas a partir de los genes del núcleo al interior de la mitocondria se den con eficacia. Este proceso está bien regulado y está mediado por un complejo de proteínas, algunas de ellas situadas en las membranas externa (TOM) e interna (TIM) de la mitocondria. Aunque el mecanismo completo de transporte no está bien definido todavía en mamíferos, sí es posible que según sean las necesidades de transporte de material al interior de la mitocondria, la actividad contráctil actúe de una forma más o menos directa sobre el incremento de la transcripción de los elementos que participan en el mismo, como se ha visto en algunos estudios en ratones (3). En el caso contrario, donde se genera un desuso crónico de la musculatura es posible que este proceso esté relacionado con muchos de los desequilibrios metabólicos que se generan, relacionados con el cambio en ROS producto de un bajo estímulo muscular, pudiendo influir en un mal transporte al interior mitocondrial. Algunas investigaciones apuntan a la gran relación que tiene la disfunción mitocondrial crónica con diversas patologías metabólicas, neurodegenerativas e, incluso cáncer(4). Es tan sencillo como comprender que si el conjunto de mitocondrias no funciona correctamente, la célula no podrá obtener la energía necesaria para realizar sus funciones vitales.
El ambiente celular es un complejo sistema de moléculas con funciones bien determinadas que son activadas o inhibidas dependiendo de los estímulos percibidos. En este caso, el contenido mitocondrial del músculo está muy asociado a las condiciones de uso del mismo viéndose que el ejercicio físico a una intensidad y/o volumen determinado es un estímulo muy potente para estimular la síntesis de contenido proteico concreto que mejore la funcionalidad mitocondrial. En realidad, la célula (en condiciones no patológicas) se adapta a las señales que recibe, sobre todo aquellas que se mantienen en el tiempo, para poder responder mejor ante las circunstancias ambientales, por lo que existen ciertos estímulos provocados por la activación muscular que influyen sobre determinadas proteínas y hacen que las mismas respondan activando otras proteínas o factores de transcripción que llegarán al lugar concreto y transmitirán ese mensaje de “es necesario generar más energía”.
Una de las proteínas más conocidas en relación con la biogénesis mitocondrial y con otros procesos metabólicos importantes es el “peroxisome proliferator-activated receptor-g coactivator 1a”, o más conocido como PGC-1a. Está relacionado con la regulación de algunos factores de transcripción importantes, como Tfam, o de la superóxido dismutasa 1 y 2 y de catalasa, que actúan como antioxidantes. También se ha visto relación entre la sobreexpresión de PGC-1a y el incremento de fibras tipo-I, siendo una forma más de adaptación de la célula al ambiente.
El estímulo generado por el ejercicio de resistencia hace que haya modificaciones en el interior celular, con cambios en las concentraciones de Ca2+ e incrementándose el ratio AMP/ATP, entre otros. Estos elementos activan proteínas concretas que generan la activación de determinados elementos, entre ellos la PGC-1a, a través de proteínas de unión y otros factores de transcripción, como CREB, MEF2, p38, etc. Además, esa diferencia entre AMP/ATP genera una activación de AMPK, una proteína activada por AMP, lo que genera la fosforilación directa de PGC-1a, potenciando su actividad. (Para ampliar esta información, se recomienda la lectura del siguiente Blog: “ Introducción a la Biogénesis Mitocondria Estimulada por Ejercicio ")
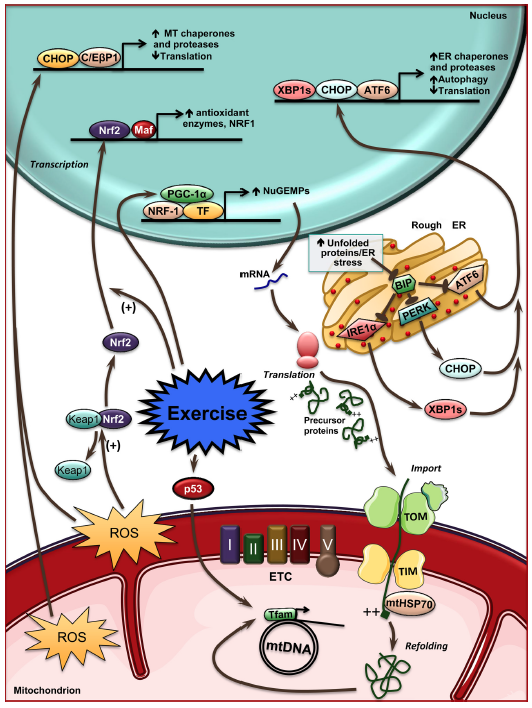
(Erlich et al., 2016)
Sin embargo, lo que es mucho más interesante es que AMPK activa el promotor del gen Pgc-1a, aumentando la expresión de la proteína PGC-1a. Sin embargo, algunas investigaciones han mostrado la existencia de variantes diferentes dependiendo del exón a partir del cual se produzca la transcripción. Estos resultados son de gran interés dado que es posible que dependiendo del estímulo concreto que se genere, de forma resumida sea ejercicio de resistencia o fuerza, el producto que se generará tras la transcripción será diferente en longitud y, por tanto, en funcionalidad, dependiendo de a partir de qué exón del Pgc-1a comience la transcripción(5). Una isoforma u otra de esta proteína generará una adaptación celular diferente, dirigida a mejorar su capacidad de respuesta ante estímulos tan diferentes como son el ejercicio de fuerza y el de resistencia. Por tanto, esto es un ejemplo más del complejo mecanismo de respuesta existente a nivel celular, por lo que no es posible entender estos procesos desde el punto de vista tan simplista que a veces se pretende hacer. Tan importante es la isoforma que se transcribe como entender que la célula tiene sus propios objetivos vitales a los que responde. Por ello, es muy necesario conocer la dosis determinada de ejercicio, controlando las variables de intensidad o volumen, para saber qué respuesta celular se va a obtener, dado que dependiendo de esto se podrá o no conseguir el objetivo, siempre que el resto de variables, como las que se mencionarán a continuación, lo permitan.
Otro punto a destacar es la dotación genética de cada individuo, así como las situaciones ambientales a las que se expone, que hará que sus células respondan de una forma u otra. Al final, a partir del contenido genético existente se podrán sintetizar las herramientas necesarias para actuar ante un evento molecular, siempre y cuando toda la cadena necesaria esté bien regulada y funcione correctamente. Así mismo, el conocimiento sobre los diferentes mecanismos epigenéticos que alteran la expresión del genoma están adquiriendo una mayor relevancia, lo que resulta en un elemento más que interviene en la regulación de los procesos celulares, como se ha visto en algunos estudios que han mostrado un descenso en la metilación del DNA tras el entrenamiento, lo que conlleva un aumento en la transcripción(6,7).
¿Quiere decir que debido a esta gran complejidad molecular debamos olvidarnos de conocer qué ocurre en la célula? Rotundamente, NO.
Conocer la biología molecular es de vital importancia para entender porqué unos estímulos, por ejemplo en cuanto a intensidad de ejercicio, generan una respuesta y no otra, dado que en muchas ocasiones de esto depende conseguir los objetivos marcados previamente.
Determinar la dosis de ejercicio es una tarea compleja, debido a la cantidad de variables que en ella intervienen, ya que duración, frecuencia, intensidad e, incluso, los periodos de descanso intra e inter-sesión son factores que pueden influir en la respuesta celular y en la adaptación ante estímulos crónicos. Por tanto, definir y concretar el volumen total, así como ajustar el resto de variables del entrenamiento según las necesidades para cumplir un objetivo concreto es un proceso complejo que requiere una amplia investigación, donde confluyen estudios que van desde la validación de herramientas que permitan medir de una forma efectiva el ejercicio aplicado a otros más relacionados con las cascadas de señalización y los eventos moleculares específicos relacionados con la intervención realizada.
Como se puede intuir conociendo las funciones de la mitocondria, generalmente la biogénesis mitocondrial se relaciona preferentemente con determinados ejercicios de resistencia, así como se ha visto también que algunas estrategias nutricionales y otras variables pueden influir en este proceso.
A la hora de estudiar qué ocurre en el interior de la célula, existen ciertas limitaciones cuando se pretende medir el contenido mitocondrial, además de la dificultad para controlar las variables relativas al ejercicio antes mencionadas y determinar qué tipo de intervención se va a realizar. Algunos estudios relevantes sobre este tema se han realizado en ciclistas por medio del control de la producción de potencia máxima (Wmax) y del VO2max, pudiéndose observar que tanto la intensidad del ejercicio como el volumen son variables con una gran relevancia para desencadenar esta respuesta mitocondrial. En algunos casos, se ha podido ver que sprints interválicos de alta intensidad generan un aumento más significativo del contenido nuclear de proteína PGC-1a, frente a otros de menor intensidad, por lo que es posible que esta variable sea mucho más relevante que el volumen, a efectos de incrementar la biogénesis mitocondrial(6,7), o al menos la relación entre volumen e intensidad , pueda ser un factor determinante para potenciar algunas respuestas moleculares.
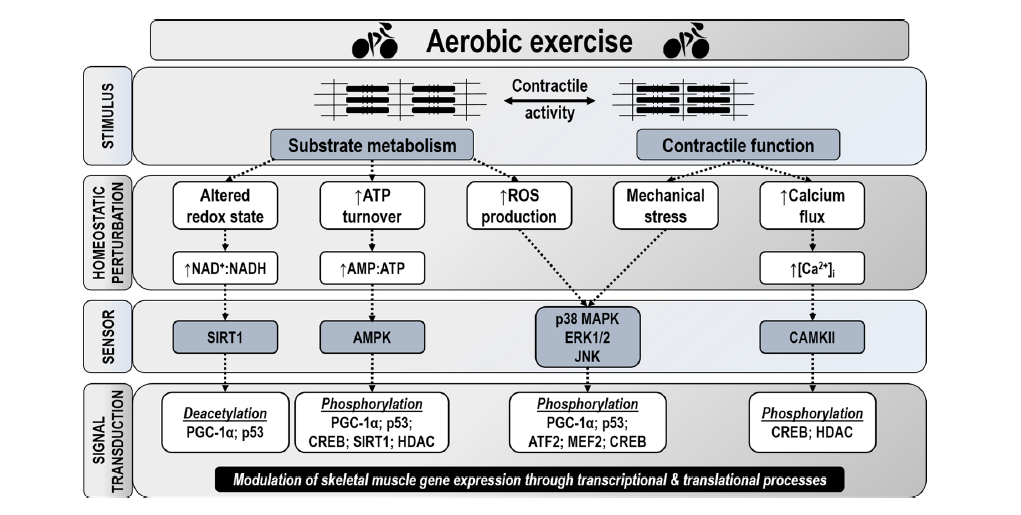
(Granata et al., 2018)
Somos el producto del funcionamiento de nuestras células ante la respuesta a todos los elementos que llegan a ella, tanto externos como internos. Sin embargo, todavía no sabemos con precisión cómo funcionamos, qué respuesta se generará tras un programa de ejercicio, tras la ingesta de determinados nutrientes o cómo afecta el propio descanso, entre infinitos estímulos posibles. Y, ante todos estos elementos que no controlamos, pretendemos sacar conclusiones generalistas (o más bien, sensacionalistas) que resuman un flujo complejo de eventos moleculares que todavía no conocemos en profundidad. La investigación avanza cada día, añadiendo una pieza más al puzzle, reemplazando otras que se descubre no encajaban a la perfección y generando muchas otras incógnitas que permiten desarrollar nuevas investigaciones, mucho más precisas, de las que se puedan sacar conclusiones un poco más acertadas, siempre en un contexto determinado y controlado.
En conclusión, la biogénesis mitocondrial es un proceso muy importante relacionado con la mejora de la funcionalidad del músculo esquelético, pero que además, es objeto de interés no solo en rendimiento deportivo, sino a nivel de mejora de ciertas condiciones patológicas, debido a su gran relación con la actividad muscular. El sedentarismo es una lacra social cada vez más extendida y ampliamente relacionada con procesos patológicos y con el desarrollo de enfermedades crónicas no transmisibles. Entender que las mitocondrias se “desconfiguran” con el desuso es uno de los elementos a tener en cuenta a la hora de responder a esa pregunta de porqué hay que generar programas de ejercicio adecuados y, sobre todo, de porqué es necesario definir la dosis a la que se debe prescribir ese ejercicio, ya que todos los indicios apuntan a la gran relación con el buen funcionamiento mitocondrial. Sin embargo, es necesario tener en cuenta que muchas de las conclusiones a las que llega la investigación son por el estudio de individuos sanos donde se aplica un determinado tipo de ejercicio. Pero, ¿Qué ocurre en el organismo de una persona con obesidad? ¿Cómo se encuentran alterados estos mecanismos? ¿Qué ha ocurrido en la mitocondria y en todos los elementos relacionados con ella? ¿Qué proteínas o factores de transcripción prevalecen en el ambiente celular de la obesidad? Son muchos aspectos a tener en cuenta a la hora de tratar ciertas patologías, ampliando el punto de vista a lo establecido hasta ahora.
En el caso de la obesidad la pérdida de peso es un factor clave y a tener en cuenta, pero no vale cualquier aproximación, dado que no todo soluciona el problema desde el punto fisiológico y celular. La pérdida de peso únicamente basándonos en una reducción de la ingesta calórica se ha visto no es tan metabólicamente efectivo como la dieta y el ejercicio unidos(4), sin embargo ¿Cualquier dieta vale? ¿Cualquier programa de ejercicio genera las mismas modificaciones metabólicas? Está claro que no.
Una nutrición adecuada y la adquisición de unos hábitos saludables ayuda a mejorar ese ambiente celular patológico existente para que, en base a lo que se ha visto, sea el ejercicio físico el que genere cambios tanto en el contenido mitocondrial, ajustando el volumen del entrenamiento, y cambios en la funcionalidad de las mitocondrias, asociado a la intensidad(7). Definir, combinar y controlar adecuadamente estas dos variables, junto con establecer el abordaje nutricional es posiblemente una de las claves que ayudará a los profesionales a generar protocolos concretos y efectivos para dar solución a esta patología, que, incluso bajo ese alteración del ambiente, continúa habiendo una plasticidad mitocondrial que permite revertir el proceso hacia una situación saludable.
Las características fisiológicas, celulares y físicas que tiene las patologías tan complejas como, por ejemplo la obesidad, hacen que no todo sea aplicable a la práctica, por lo que es necesario haya una comunicación entre profesionales, una definición del contexto celular en el que nos movemos en cada momento y de la integración de todos los eventos moleculares que se generan ante determinados estímulos. Por tanto, es vital contextualizar cada avance que nos ofrece la investigación y seguir caminando hacia un mayor conocimiento que nos brindará la clave para entender el lenguaje celular que, al fin y al cabo es lo que nos compone.
Bibliografía:
1. Triolo M, Hood DA. Mitochondrial breakdown in skeletal muscle and the emerging role of the lysosomes. Arch Biochem Biophys. 12 de noviembre de 2018;
2. Ould Amer Y, Hebert-Chatelain E. Mitochondrial cAMP-PKA signaling: What do we really know? Biochim Biophys Acta Bioenerg. 2018;1859(9):868-77.
3. Erlich AT, Tryon LD, Crilly MJ, Memme JM, Moosavi ZSM, Oliveira AN, et al. Function of specialized regulatory proteins and signaling pathways in exercise-induced muscle mitochondrial biogenesis. Integr Med Res. septiembre de 2016;5(3):187-97.
4. Toledo FGS, Goodpaster BH. The role of weight loss and exercise in correcting skeletal muscle mitochondrial abnormalities in obesity, diabetes and aging. Mol Cell Endocrinol. 15 de octubre de 2013;379(1-2):30-4.
5. Silvennoinen M, Ahtiainen JP, Hulmi JJ, Pekkala S, Taipale RS, Nindl BC, et al. PGC-1 isoforms and their target genes are expressed differently in human skeletal muscle following resistance and endurance exercise. Physiol Rep [Internet]. 5 de octubre de 2015 [citado 18 de noviembre de 2018];3(10). Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC46329...
6. Granata C, Jamnick NA, Bishop DJ. Principles of Exercise Prescription, and How They Influence Exercise-Induced Changes of Transcription Factors and Other Regulators of Mitochondrial Biogenesis. Sports Med. 2018;48(7):1541-59.
7. Bishop DJ, Granata C, Eynon N. Can we optimise the exercise training prescription to maximise improvements in mitochondria function and content? Biochim Biophys Acta. abril de 2014;1840(4):1266-75.
