Resumen
La suplementación de ácidos grasos poliinsaturados omega-3 (N-3) se ha asociado con efectos secundarios reducidos y una mejor calidad de vida (QOL) en pacientes con cáncer de mama que reciben quimioterapia. El estudio actual informa los resultados secundarios del ensayo controlado aleatorizado de DHA que fue diseñado para evaluar la suplementación con ácido docosahexaenoico (DHA) (4.4 g/día) junto con seis ciclos de quimioterapia neoadyuvante (NAC) (3 semanas/ciclo) en mujeres con cáncer de mama no metastásico (N = 49). El objetivo del estudio actual fue evaluar los efectos de la suplementación con DHA en la calidad de vida y el comportamiento de ejercicio en mujeres sometidas a NAC para el cáncer de mama. Se utilizaron cuestionarios autoadministrados para medir la calidad de vida y el comportamiento del ejercicio antes de comenzar la quimioterapia (línea de base), antes de cada ciclo de quimioterapia (ejercicio) y después de completar la quimioterapia. La suplementación con DHA no afectó significativamente la calidad de vida, el volumen de ejercicio aeróbico o la frecuencia de entrenamiento de resistencia durante el tratamiento. Sin embargo, el volumen medio de ejercicio aeróbico fue significativamente más bajo en la semana 12 (-53.5 minutos/semana; IC 95%, -100.5 a -6.3; p = 0.02) y la semana 18 (-70.8 minutos/semana; IC 95%, -123.0 a -18.6; p = 0.01) en comparación con la base. La frecuencia de entrenamiento de resistencia media fue menor en la semana 12 (-0.57 veces/semana; IC 95%, -1.0 a -0.13; p = 0.02) en comparación con la línea de base. Las pautas de ejercicio para cumplir durante la quimioterapia no se asociaron con una mejor calidad de vida. En el estudio exploratorio actual, la calidad de vida y el ejercicio disminuyeron durante el tratamiento, independientemente de la suplementación con DHA, destacando la necesidad de cuidados de apoyo y posibles terapias que puedan mitigar estas disminuciones en pacientes con cáncer de mama que reciben NAC. Se necesitan estudios con alimentación adecuada para determinar si la suplementación con DHA mejora estos dos índices de salud. El ensayo está registrado en ClinicalTrials.gov (NCT03831178).
Introducción
Se estima que 2,3 millones de mujeres fueron diagnosticadas con cáncer de seno en 2022, lo que lo convierte en el segundo cáncer más común en todo el mundo (1). La quimioterapia neoadyuvante (NAC) se usa para tratar a las mujeres con cáncer de mama operable en etapa temprana para mejorar los resultados de resección quirúrgica (2). NAC se prescribe con mayor frecuencia a pacientes con subtipos más agresivos que incluyen cáncer de mama triple negativo y cáncer de mama HER2 + (3,4). El tratamiento para el cáncer de mama no metastásico con frecuencia implica quimioterapia sistémica preoperatoria (neoadyuvante) antes de la eliminación quirúrgica del tumor (4). La calidad de vida relacionada con la salud (QOL) considera cómo la enfermedad y el tratamiento afectan el sentido de la función general y el bienestar de un individuo (5). La calidad de vida se ha convertido en una medida de resultado importante y un factor en las decisiones de tratamiento para NAC (6,7). Se informa que el tratamiento con quimioterapia se asocia con varios efectos secundarios físicos y psicosociales que incluyen náuseas, vómitos, fatiga, función cognitiva deteriorada y dolor que influyen en la calidad de la calidad de vida y el ejercicio (6–11). Todo esto contribuye a una reducción de la tolerabilidad al tratamiento y a los peores resultados clínicos (12).
Se ha informado que la suplementación de ácidos grasos poliinsaturados de cadena larga omega-3 (N-3) a las mujeres que reciben otros regímenes de quimioterapia dan como resultado una reducción de algunos efectos secundarios de quimioterapia, incluida la modulación de perfiles inflamatorios, reducción de los efectos secundarios gastrointestinales, el mantenimiento del músculo esquelético y la recuperación neuronal mejorada ((recuperación neuronal mejorada ((13). Una revisión reciente de Newell et al. (2021) concluyeron que la suplementación de ácidos grasos poliinsaturados de cadena larga N-3 en la terapia clínica del cáncer mejoró la calidad de vida general entre pacientes con varios tipos de cáncer (14). Sin embargo, estos estudios no informaron sobre las mujeres que recibieron NAC.
Actualmente no existen recomendaciones dietéticas específicas para ácidos grasos poliinsaturados de cadena larga durante la terapia del cáncer o la supervivencia. Nuestro grupo ha demostrado que la alimentación de dietas complementadas con el ácido graso poliinsaturado de cadena larga N-3, ácido docosahexaenoico (DHA), reduce el crecimiento tumoral y mejora la eficacia de la quimioterapia (15). No se han estudiado los efectos sobre la calidad de vida o la capacidad de ejercicio. Aunque se ha demostrado que el ejercicio es beneficioso para aliviar los efectos secundarios y mejorar la calidad de vida durante la quimioterapia (9), no hay recomendaciones clínicas. Sin embargo, en base a los efectos protectores del ejercicio sobre la mortalidad, la Organización Mundial de la Salud (OMS) recomienda que los sobrevivientes de cáncer realicen al menos 150-300 minutos de actividad física aeróbica de intensidad moderada por semana, así como actividades de fortalecimiento muscular dos o más días por semana (16).
El objetivo del manuscrito actual fue evaluar los efectos de la suplementación con DHA y el NAC en la calidad de vida autoinformada y el comportamiento de ejercicio en mujeres sometidas a tratamiento con cáncer de seno. Estos representan análisis de resultados secundarios del ácido docosahexaenoico para mujeres con cáncer de mama en el ensayo controlado aleatorizado (DHA WIN) (DHA) (DHA) (DHA)17).
Materiales y métodos
Entorno y participantes
El protocolo para el RCT DHA Win, incluidos los criterios de inclusión y exclusión, se ha publicado previamente (17). El ensayo incluyó a las mujeres con cáncer de mama no metastásico en estadio I-III que prescribió quimioterapia neoadyuvante. Los participantes fueron reclutados por oncólogos y enfermeras de ensayos clínicos en el Cross Cancer Institute (Edmonton, Alberta, Canadá) y se examinó la elegibilidad. El RCT DHA Win recibió la aprobación de Health Canada (#HC6–24-C220167) y la aprobación ética completa de la Junta de Ética de Investigación de Salud de Alberta-Comité de Cáncer (HREBA.CC-18-0381) (17). El consentimiento informado por escrito se obtuvo antes de la participación de las personas en el estudio. El tamaño de muestra objetivo de 26 participantes por brazo de tratamiento se determinó en función del resultado primario del ensayo (cambio en el índice Ki67 en el tumor).
Diseño y procedimientos de estudio
El ensayo DHA Win fue un ECA de fase II doble de brazo, doble ciego, diseñado para investigar los efectos de la suplementación con DHA concomitante con la quimioterapia neoadyuvante en mujeres con cáncer de mama no metastásico (17). Todas las mujeres recibieron quimioterapia estándar de atención, que fue uno de los dos regímenes de quimioterapia neoadyuvante basados en docetaxel que se usaron en esta población. Cada régimen consistió en seis ciclos de quimioterapia que se administraron en intervalos de 3 semanas (durante un total de 18 semanas). Los cuestionarios de calidad de vida se completaron al inicio (semana 0) y al final del ciclo 6 (semana 18). Los cuestionarios de ejercicio se completaron al comienzo de cada ciclo de 3 semanas y al final del ciclo 6 (semana 18). Los participantes recibieron copias en papel de los cuestionarios para completar durante las visitas a la clínica.
Aleatorización
La aleatorización de bloque ocurrió como se describió anteriormente (17). Brevemente, un bioestadístico generó una lista de aleatorización de pacientes y números aleatorios de botellas que utilizan aleatorización adaptativa covariable. La lista de botellas aleatorizada se proporcionó a los productos nutricionales DSM para fines de etiquetado, así como al Coordinador de ensayos clínicos sin cebar (CTC) y farmacéutico. La base de datos REDCAP se utilizó para asignar a los participantes a un brazo de estudio y proporcionar un identificador de estudio único por parte del coordinador del estudio. El personal de farmacia asignó números de botellas basados en el brazo de tratamiento en el primer día de cada ciclo de quimioterapia. El coordinador del estudio ingresó a la ID de la botella en la base de datos REDCAP. Los participantes, patólogos, médicos e investigadores fueron cegados durante todo el juicio. El CTC, estadístico y farmacéutico no tenían brecha. Los suplementos DHA y placebo eran idénticos en tamaño, forma, color, textura y botellas.
Intervención
Los participantes fueron aleatorizados para recibir 4,4 g/día de DHA o un suplemento placebo (17). El Grupo DHA recibió once cápsulas de aceite de triglicéridos de algas enriquecidas con algas (Life’sDHA S40-O400), mientras que el grupo de placebo recibió once cápsulas de 1 g de una mezcla de aceite de maíz/soja por día (DSM Nutricional Products, Columbia, Maryland, USA). El suplemento placebo contenía cantidades iguales de ácidos grasos poliinsaturados como suplemento DHA, en forma de ácido linoleico. Los participantes recibieron instrucciones de consumir oralmente las cápsulas en cualquier momento durante el día, con o sin comida. La intervención comenzó al comienzo del primer ciclo de quimioterapia y continuó durante el tratamiento de quimioterapia. El cumplimiento se determinó mediante una revisión del diario de dosificación del paciente y el número registrado de las cápsulas restantes devueltas al final del estudio.
Evaluación de la calidad de vida y el comportamiento del ejercicio
Los cuestionarios para registrar la calidad de vida y el comportamiento del ejercicio se dieron a los participantes antes de comenzar la quimioterapia (línea de base), antes de cada ciclo de quimioterapia (ejercicio) y después de completar la quimioterapia. Los participantes recibieron instrucciones sobre cómo llenarlos, pero no había un método utilizado para garantizar la precisión de las respuestas. La calidad de vida y la fatiga específicas del cáncer se evaluaron utilizando la evaluación funcional de la terapia del cáncer (hecho)-general (FACT-G) (18,19), Hecho-mama (FACT-B) (20,21), Hecho – Taxane (22,23), Hecho-síntomas endocrinos (hecho) (24,25) y la evaluación funcional de la terapia de enfermedades crónicas (facit)-escalas de fatiga (fatiga facit) (26,27). Los puntajes más altos indican una mejor calidad de vida (y menos fatiga) entre las escalas antes mencionadas. El funcionamiento psicosocial se evaluó utilizando la escala de estrés percibida (PSS) (con puntajes más altos que indican un mayor estrés) (28), el cuestionario de emociones de Fordyce (con puntajes más altos que indican una mayor felicidad) (29), y versiones modificadas del Centro para la Escala de depresión de estudios epidemiológicos (CES-D) (con puntajes más altos que indican una mayor sintomología depresiva) (30) y el inventario de ansiedad del rasgo de estado (STAI) (con puntajes más altos que indican una mayor ansiedad) (31).
Se usó una versión adaptada del cuestionario de ejercicio de tiempo libre Godin para recopilar información sobre la frecuencia y la duración promedio del ejercicio aeróbico de luz, moderado y vigoroso, así como entrenamiento de resistencia/resistencia por semana (32,33). El ejercicio aeróbico semanal promedio se determinó agregando los minutos promedio de ejercicio aeróbico moderado a dos veces los minutos promedio de ejercicio aeróbico vigoroso. Se promediaron el volumen de ejercicio aeróbico y la frecuencia de entrenamiento de resistencia (excluyendo los niveles de referencia) y se utilizaron para clasificar a los participantes sobre la base de las recomendaciones de ejercicio de la OMS (≥ 150 minutos/semana de ejercicio aeróbico y ≥ 2 veces/semana de entrenamiento de resistencia) (16).
Análisis estadísticos
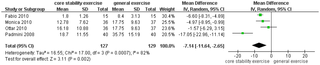
Las estadísticas descriptivas que incluyen medias (DE) y proporciones (frecuencias) se usaron para describir variables continuas y categóricas, respectivamente. Los valores basales se compararon entre grupos utilizando la prueba t independiente para variables continuas y la prueba de chi cuadrado para variables categóricas. Las muestras faltantes estaban completamente al azar y, por lo tanto, se excluyeron del análisis. Un participante en el grupo placebo no tenía datos de calidad de vida disponibles al final del tratamiento. Las leyendas de Figuras 2 y 3 Muestre el menor número de participantes con datos, ya que este número varió en cada punto de tiempo. El análisis de la covarianza se utilizó para examinar los efectos del tratamiento con DHA en las puntuaciones de la calidad de vida, así como las asociaciones entre las clasificaciones de ejercicio y las puntuaciones de la calidad de vida. El método de estimación generalizada (GEE) se utilizó para evaluar los efectos del tiempo y el tratamiento con DHA en el volumen promedio de ejercicio aeróbico y la frecuencia promedio de entrenamiento de resistencia. El método GEE se utiliza para analizar los datos correlacionados y evaluar la variabilidad entre y dentro del sujeto para los datos de medidas repetidas, y proporciona estimaciones de parámetros imparciales y errores estándar robustos. Las comparaciones de punto de tiempo se realizaron a los niveles basales de ejercicio. Se realizaron análisis tanto no ajustados como ajustados. Para el análisis ajustado, los modelos GEE se ajustaron por edad, IMC y valor basal del resultado. Los análisis post hoc no se ajustaron para comparaciones múltiples. Por lo tanto, los resultados de este estudio deben interpretarse como exploratorios. La significación estadística se definió como un valor p de dos lados <0.05. Estadístico...