Resumen
Antecedentes
El entrenamiento del ejercicio de resistencia progresiva (PRT) mejora el funcionamiento físico en pacientes con infección por VIH. La suplementación de creatina puede aumentar los beneficios derivados del entrenamiento en atletas y mejorar la función muscular en pacientes con desgaste muscular. El objetivo de este estudio fue determinar si la suplementación con creatina aumenta los efectos de la PRT sobre la fuerza muscular, la energía y la composición corporal en pacientes infectados por el VIH.
Metodología/Hallazgos principales
Este es un estudio aleatorizado, doble ciego, controlado con placebo, clínico, basado en el centro ambulatorio, ambulatorio en San Francisco. 40 hombres VIH positivos (20 creatina, 20 placebo) inscritos en un estudio de 14 semanas. Los sujetos fueron asignados al azar para recibir monohidrato de creatina o placebo durante 14 semanas. El tratamiento comenzó con una dosis de carga de 20 g/día o un número equivalente de cápsulas de placebo durante 5 días, seguido de una dosificación de mantenimiento de 4.8 g/día o placebo. A partir de la semana 2 y continuando hasta la semana 14, todos los sujetos se sometieron a un ejercicio de resistencia supervisado de tres veces por semana mientras continúan con el medicamento de estudio asignado (con ciclos repetidos de 6 semanas de carga y mantenimiento). Las principales mediciones de resultados incluyeron fuerza muscular (un máximo de repetición), Enérgica (31P espectroscopía de resonancia magnética), composición y tamaño (resonancia magnética), así como la composición total del cuerpo (absorptiometría de rayos X de doble energía). Treinta y tres sujetos completaron el estudio (17 creatina, 16 placebo). La fuerza aumentó en los 8 grupos musculares estudiados después de la PRT, pero este aumento no aumentó por suplementación con creatina (aumento promedio 44 frente a 42%, diferencia 2%, IC 95%−9.5%a 13.9%) en creatina y placebo, respectivamente). No hubo diferencias entre los grupos en los cambios en la energía muscular. El área transversal del músculo del muslo aumentó después del ejercicio de resistencia, sin ningún efecto aditivo de la creatina. La masa corporal magra (LBM) aumentó en un grado significativamente mayor con la creatina.
Introducción
En las personas con infección por VIH y otras enfermedades crónicas, el mantenimiento o el aumento de la masa muscular es importante para preservar el estado funcional y la progresión de la enfermedad sin embargo. (1). El entrenamiento del ejercicio de resistencia progresiva (PRT), ya sea solo o en combinación con el entrenamiento con ejercicio aeróbico, puede aumentar la masa muscular y mejorar el rendimiento físico en personas con infección por VIH (2)–(10). Muchas personas emplean las llamadas ayudas ergogénicas, incluidas sustancias como esteroides anabólicos y hormona del crecimiento, para facilitar la acumulación muscular y mejorar el efecto anabólico de PRT en la composición corporal con vistas a las mejoras funcionales y estéticas (11), (12). El monohidrato de creatina es un suplemento nutricional que se ha demostrado que mejora la disponibilidad de energía a corto plazo durante el ejercicio intenso y para mejorar la recuperación entre los episodios de ejercicio intensos (13), (14). Basado en tales hallazgos, los atletas competitivos y recreativos lo utilizan como una ayuda ergogénica para mejorar su eficiencia de entrenamiento. Aunque en algunas poblaciones se ha demostrado que la suplementación de creatina mejora la fuerza isotónica (15)par (16) y poder (17) Otros estudios no han podido mostrar tales efectos (18)–(21).
Hasta la fecha, no ha habido estudios específicos sobre la eficacia del uso médico de la suplementación con creatina en personas con infección por VIH. Además, los efectos de la suplementación con creatina en combinación con PRT sobre la energía muscular (por ejemplo, la función mitocondrial, la resistencia a la fatiga o el contenido de grasa intramuscular) no se conocen en la población del VIH, a pesar de que estos se consideran los principales beneficios de la suplementación de creatina. El presente estudio fue diseñado para probar la hipótesis de que el uso médico de la suplementación con creatina aumentaría los aumentos en la fuerza muscular derivada de la PRT en adultos VIH positivos. También se evaluaron el impacto funcional y los mecanismos potenciales de estas ganancias de resistencia.
Métodos
Protocolo
El protocolo para esta lista de verificación de consorte de prueba y prueba está disponible como información de respaldo; ver Lista de verificación S1 y Protocolo S1.
Ética
El estudio fue aprobado por los Comités de Investigación Humana en la Universidad de California en San Francisco y en el Centro Médico de VA de San Francisco. Todos los sujetos dieron consentimiento informado por escrito.
Participantes
Cuarenta y tres estables clínicamente estables, sujetos con VIH sedentarios (42 hombres, 1 mujer) que viven en el Área de la Bahía de San Francisco fueron reclutados por los coordinadores de nuestro estudio y estudiados entre agosto de 2001 y enero de 2004 (Figura 1). Los sujetos que usaban la terapia antirretroviral (ART) debían estar en regímenes estables durante al menos 30 días antes de la inscripción y se les pidió que permanecieran así durante el estudio. Los sujetos que no habían recibido arte por los 30 días anteriores y no tenían planes de iniciar la terapia durante el estudio también fueron elegibles.
Los criterios de exclusión incluyeron entrenamiento regular de ejercicio de resistencia, uso de hormonas anabólicas y otras putativas ayudas ergogénicas (por ejemplo, aminoácidos, suplementos de proteínas, agonistas β), creatinina sérica> 1.5 mg/dL; historia de la enfermedad renal; creatina quinasa (CK)> 1.5 veces el límite superior de lo normal (ULN); hemoglobina <8,5 g/dL; Niveles de transaminasa hepática o lactato deshidrogenasa ≥5 × Uln; diarrea no controlada, náuseas o vómitos; ingesta de alimentos orales alterados; hipogonadismo no tratado; uso farmacológico de terapias anabólicas o inmune moduladoras; infección sistémica dentro de los 30 días; antecedentes de enfermedad cardíaca; y embarazo o lactancia actual. Los sujetos en reemplazo de testosterona estable durante ≥6 meses fueron elegibles.
Tamaño de muestra
Los cálculos del tamaño de la muestra se basaron en otros estudios con un diseño similar y permiten una detección de tamaños de efecto estandarizados de 0.9 con 80% de potencia para detectar cambios en los niveles de fosfocreatina intramuscular (PCR).
Aleatorización
Los sujetos fueron aleatorizados, de manera cegada 1∶1, para recibir cápsulas de aparición idéntica que contenían monohidrato de creatina pura o placebo (ambas proporcionadas por Jarrow Universal Herbs Inc., Union City, CA) durante 14 semanas (Figura 1). Un consultor estadístico preparó una lista de aleatorización generada por computadora y se entregó directamente a la farmacia de investigación en el Hospital General de San Francisco (SFGH), donde las cápsulas fueron embotelladas y dispensadas. Todos los datos fueron recopilados y analizados sin conocimiento de la asignación de tratamiento.
Tres sujetos (1 creatina, 2 placebo), incluida la única mujer, se retiraron después de la aleatorización pero antes de la prueba de referencia o el inicio del tratamiento y, por lo tanto, se excluyen del análisis.
Intervención
Los sujetos comenzaron con una dosis de carga de 20 g/día (dividida entre cuatro dosis) o un número equivalente de cápsulas de placebo durante 5 días, seguido de una dosificación de mantenimiento de 4.8 g/día (en dos dosis de 2.4 g) o placebo. La dosificación de mantenimiento se interrumpió brevemente para ciclos de carga adicionales de 5 días al comienzo de las semanas 7 y 13. Este régimen de dosificación es similar al empleado en varios estudios recientes (según lo revisado por Nissen (13)). A los sujetos se les dio una bebida de jugo de fruta no factorativa que contenía 20 g de carbohidratos simples para tomar con cada dosis de medicación de estudio (22).
Régimen de entrenamiento.
Después de dos semanas, todos los sujetos comenzaron un programa de 12 semanas de PRT supervisado, mientras continuaban con su medicamento de estudio asignado. El entrenamiento se realizó utilizando un sistema de acondicionamiento físico de múltiples gimnasios 5000 (San Diego, CA). Los sujetos ejercieron durante 1½ horas 3 días por semana durante 12 semanas. El entrenamiento incluyó dorsiflexión del tobillo, flexión plantar del tobillo, flexión plantar del tobillo con rodilla doblada, prensa de piernas, rizos en las piernas, ejercicios de tórax PEC, empuje de tríceps, rizo de bíceps y tres tipos de abdominales. La fuerza en cada grupo muscular se evaluó mediante una prueba máxima de repetición (1RM) (23) Excepto en el Recto Abdomino, en el que se registró el número de abdominales realizados en 30 segundos. Cada sesión de entrenamiento incluyó 4 series de 8 repeticiones al 80% de los 1RM para cada ejercicio. El 1RM para cada ejercicio se reevaluó una vez cada dos semanas y la intensidad de entrenamiento se ajustó para mantener el 80% del 1RM. Todas las mediciones se realizaron después de dos días de descanso en ausencia de cualquier síntoma de dolor muscular o fatiga.
Objetivos
El objetivo principal era comparar los cambios en la fuerza muscular (1RM, las sentadillas y el MVC) de la semana 0 a la semana 14 en los dos grupos de tratamiento. Los objetivos secundarios eran comparar cambios en el tamaño muscular, la composición, la energía y la fatiga, así como la composición corporal y la bioquímica.
Mediciones de resultados
Los sujetos fueron estudiados en el Centro General de Investigación Clínica (GCRC) en SFGH y en la Unidad de Resonancia Magnética en el Centro Médico de San Francisco VA. La altura y el peso se registraron con sujetos con un vestido de hospital. Las mediciones de la fuerza muscular, el tamaño, la composición, la energía y la fatiga, así como el peso corporal y la composición y los bioquímicos séricos, se realizaron al inicio, después de dos semanas de tratamiento con creatina o placebo (antes de que comenzara PRT), y nuevamente después de 12 semanas de PRT (semana 14). La seguridad fue monitoreada durante todo el estudio.
Enérgica y fatiga muscular.
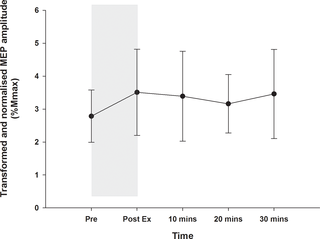
Medidas no invasivas de fosfocreatina intracelular (PCR), fósforo inorgánico (PI) y pH se obtuvieron del músculo dorsiflexor del tobillo derecho por 31P espectroscopía de resonancia magnética (MRS) utilizando un imán de Oxford superconductor de 1,9 t de 30 cm, como se describe en detalle en otra parte (24), (25). Los sujetos realizaron dos protocolos de contracción el mismo día, separados por 20 minutos de descanso. El primer protocolo consistió en una contracción voluntaria máxima (MVC) de 15 segundos, que se utilizó para determinar la capacidad del músculo para la fosforilación oxidativa (24) reportado como el medio tiempo (t1/2) de recuperación de PCR después de la contracción. El análisis de recuperación indicó que nuestro sistema MRS puede detectar cambios de PCR de 0,5 mm. El segundo protocolo se usó para evaluar la función muscular durante condiciones fatigantes de alta intensidad. La fuerza muscular y la energía se midieron simultáneamente durante 36 MVC consecutivos durante 6 minutos, uno cada 10 segundos. El perfil de fatiga se calculó según lo descrito por Karatzaferi et al. (26).
Fuerza del dorsiflexor.
La fuerza MVC isométrica se registró durante la dorsiflexión del tobillo, mientras que la pierna se colocó en el imán para los estudios MRS (24), (25) La fuerza más alta de los 3 MVC se usó para cuantificar la resistencia a la dorsiflexión (24) y el rendimiento de la escala durante la tarea de fatiga antes mencionada.
Tamaño muscular y composición.
Protón t1-Se se usó imágenes de resonancia magnética ponderada (MRI) para visualizar el área de sección transversal (CSA) del muslo y el ternero utilizando un sistema de visión magnetoma de Siemens de 1,5 t de cuerpo entero, como se describió anteriormente (24). Los datos se analizaron utilizando un programa de software personalizado (Interactive Data Language Research Systems, Inc., Boulder, CO). El coeficiente de variación de las mediciones de CSA muscular fue del 0,6%.
Composición corporal.
Cuerpo entero y grasa regional y masa corporal magra (LBM) se midieron utilizando un modelo de rayos X de doble energía DPX Lunar DPX (DEXA) (Madison, WI) (27), (28).
Mediciones bioquímicas.
Se recogieron muestras de sangre en ayunas para determinar los niveles de creatina en plasma y lactato y creatinina sérica, creatina quinasa (CK), lípidos, glucosa e insulina. La creatina en plasma se determinó mediante cromatografía líquida: espectrometría de masas en tándem (LC/MS) utilizando un topógrafo LC interfacido con un TSQ Quantum Ultra Triple Stage Quadrupol MS (Thermo-Finnigan, San José, CA) operado en …