Resumen
Objetivo
El objetivo de esta revisión sistemática y metaanálisis fue determinar el efecto general del entrenamiento de resistencia (RT) en las medidas de fuerza muscular en personas con enfermedad de Parkinson (EP).
Métodos
Los ensayos controlados con diseño de grupo paralelo se identificaron a partir de la búsqueda de literatura computarizada y el seguimiento de las citas realizados hasta agosto de 2014. Dos revisores examinaron de forma independiente para detectar elegibilidad y evaluaron la calidad de los estudios utilizando el riesgo de coochrane de la herramienta de sesgo. Para cada estudio, se calcularon las diferencias medias (MD) o las diferencias de medias estandarizadas (SMD) y los intervalos de confianza (IC) del 95% para los resultados continuos basados en comparaciones entre grupos utilizando datos posteriores a la intervención. El análisis de subgrupos se realizó en función de las diferencias en el diseño del estudio.
Resultados
Nueve estudios cumplieron con los criterios de inclusión; Todos tenían un riesgo moderado a alto de sesgo. Los datos agrupados mostraron que la extensión de la rodilla, la flexión de la rodilla y la resistencia a la prensa de las piernas fueron significativamente mayores en pacientes con EP que emprendieron RT en comparación con los grupos de control con o sin intervenciones. Los subgrupos fueron: RT vs. Control-Intervención, RT vs. Control-Intervención, RT-Con otra forma de ejercicio vs. Control-Intervención, RT-With-Otro-Form-of-Exercise vs. Control-With-Intervention. El análisis de subgrupos agrupados mostró que la RT combinada con el ejercicio aeróbico/de equilibrio/estiramiento resultó en una extensión de rodilla significativamente mayor, flexión de la rodilla y resistencia a la prensa de las piernas en comparación con la no intervención. En comparación con la cinta de correr o el ejercicio de equilibrio, resultó en una mayor flexión de la rodilla, pero no la extensión de la rodilla o la resistencia a la prensa de la pierna. La RT sola resultó en una mayor extensión de la rodilla y resistencia a la flexión en comparación con el estiramiento, pero no en una mayor resistencia a la prensa de las piernas en comparación con la no intervención.
Discusión
En general, la evidencia actual sugiere que las intervenciones de ejercicio que contienen RT pueden ser efectivas para mejorar la fuerza muscular en personas con EP en comparación con el ejercicio. Sin embargo, dependiendo del grupo muscular y/o la dosis de entrenamiento, la RT puede no ser superior a otros tipos de ejercicio. Las intervenciones que combinan RT con otro ejercicio pueden ser más efectivas. Los resultados deben interpretarse con precaución debido al riesgo relativamente alto de sesgo de la mayoría de los estudios.
Introducción
La enfermedad de Parkinson (EP) es el segundo trastorno neurodegenerativo más común después de la enfermedad de Alzheimer (1) y afecta a aproximadamente seis millones de personas en todo el mundo (2). La EP es más frecuente en los grupos de mayor edad con un aumento rápido de casos después de la edad de 60 años (3,4). La tasa de incidencia ajustada para la edad se estima en 9.7 a 13.8 casos por cada 100,000 personas por año (5). Se espera que estos números aumenten aún más en las próximas décadas debido a un envejecimiento de la población (6).
La EP es un trastorno crónico y progresivo que se cree que es causada por la muerte de las neuronas dopaminérgicas en la sustancia negra de los ganglios basales (7). Existe evidencia emergente de que otras estructuras no dopaminérgicas también están involucradas (8). La PD incluye síntomas motor y no motores (1,9). Los síntomas no motores incluyen una disminución de la función cognitiva, problemas psiquiátricos como depresión y ansiedad, y trastornos autónomos, de sueño y sensoriales (10). Los síntomas motores comunes son el temblor, la bradicinesia (lentitud del movimiento), la rigidez, la inestabilidad postural y una postura inclinada, dificultades de la marcha, incluida la congelación de la marcha (incapacidad para iniciar el movimiento) y la debilidad muscular ((((1,2,11). Estas dificultades de movimiento conducen a niveles de actividad disminuidos en personas con EP que, a su vez, perjudica aún más la fuerza y el funcionamiento físico. La fuerza muscular deteriorada puede ser un síntoma primario inherente a la EP (12), pero esto sigue siendo controvertido (13). La fuerza deteriorada puede ser de origen central (14), ya que la capacidad de activar las neuronas motoras del músculo activo podría verse afectada debido al impulso cortical deficiente al músculo (15). Además, la debilidad muscular puede contribuir a la inestabilidad postural y las dificultades de la marcha (16,17) y ha sido identificado como una causa secundaria de bradykinesia en PD (18).
Las opciones de tratamiento disponibles para la EP incluyen terapia farmacológica (reemplazo de dopamina), cirugía cerebral (estimulación cerebral profunda (DBS) y ejercicio (1,2). Si bien no hay cura para la EP, estas terapias tienen como objetivo proporcionar alivio de los síntomas (7). Los medicamentos y la cirugía son efectivos para aliviar los síntomas cardinales (temblor, bradicinesia, rigidez). Sin embargo, la terapia farmacológica solo mejora insuficientemente los desorden de equilibrio y la marcha y puede causar efectos secundarios desactivantes que se vuelven más prominentes a medida que avanza la enfermedad (19). Los DB pueden proporcionar mejoras en el equilibrio y la marcha hasta cierto punto, pero su efectividad depende del sitio de estimulación en el cerebro y los coeficientes de medicamentos, y disminuye con el tiempo (20).
Se ha demostrado que el ejercicio es beneficioso para las personas con EP (2,21). En particular, se ha demostrado que el entrenamiento de resistencia (RT) mejora la fuerza, y algunas medidas de función física y movilidad en pacientes con EP (22–25). Además, se ha demostrado que los aumentos en la fuerza muscular en respuesta a la RT están acompañados de mecanismos adaptativos celulares como la hipertrofia de miofibra en personas con EP (26). RT también podría tener un efecto neuroprotectivo y reducir la progresión de la enfermedad (15,27) .Yet, se desconoce la evidencia de estos efectos beneficiosos de una amplia variedad de RT y se desconoce el efecto general de la RT sobre las medidas de la fuerza muscular. Actualmente, existen pocas pautas basadas en evidencia para RT para personas con PD (28). Por lo tanto, esta revisión sistemática tiene como objetivo (1) recopilar estudios que utilizaran RT para mejorar la fuerza muscular en personas con EP y actualizar revisiones anteriores, (2) determinar el efecto general de la RT sobre las medidas de la fuerza muscular en personas con EP y (3) intervenciones efectivas de RT para aumentar la fuerza en las personas con ED para proporcionar a las directrices basadas en evidencia para profesionales de la salud que prescriben RT a pacientes con PD a PD.
Métodos
Estrategia de búsqueda de literatura
La búsqueda de literatura se realizó en Medline, la Biblioteca Cochrane, Cinahl, Embase y Sportdiscus. Se combinaron las palabras de malla o clave y los sinónimos correspondientes, incluida la enfermedad de Parkinson, el entrenamiento de resistencia y los ensayos clínicos controlados. Los encabezados de los sujetos se modificaron para su uso en las otras bases de datos. Se puede encontrar una copia de la estrategia de búsqueda completa en cada base de datos en la información de soporte (Apéndice S2). Cada base de datos fue buscada desde su primer registro disponible hasta el 15 de agosto de 2014th. También se examinaron listas de referencias de todos los artículos relevantes para su identificación de estudios elegibles adicionales.
Criterios de inclusión y exclusión
La RT se definió como una forma de entrenamiento de fuerza diseñado para mejorar los componentes de la aptitud muscular, incluida la fuerza, la potencia y la resistencia. Implica la activación de unidades motoras contra una resistencia externa que puede aplicarse a movimientos de todo el cuerpo o grupos musculares aislados. Se puede utilizar una variedad de equipos para aplicar resistencia externa, por ejemplo, peso corporal, pesas libres, máquinas con pesos adicionales, bandas elásticas o presión de agua. Un programa RT está diseñado ajustando variables de entrenamiento agudo, como la elección de ejercicios, el orden de los ejercicios, la frecuencia de las sesiones de ejercicio, el número de conjuntos y repeticiones, niveles de intensidad y períodos de descanso (29,30).
Los estudios que cumplían los siguientes criterios se consideraron para la revisión: 1) los participantes del estudio tenían que tener EP (cualquier edad, cualquier terapia farmacológica concurrente, cualquier duración o gravedad de la enfermedad); 2) Al menos un grupo del estudio debe haber sufrido una intervención RT (> 2 semanas de ejercicio para ver un cambio de fuerza fisiológica, no una mejora neurológica en el reclutamiento de fibra muscular (31)); 3) se informó al menos una medida de resultado de la fuerza muscular; 4) El diseño del estudio fue un diseño grupal paralelo de algún tipo (es decir, incluyó al menos dos brazos con un grupo de intervención que realizó RT y un grupo de control que no recibió tratamiento que no sea la práctica médica estándar o se sometió a otro tipo de intervención que no incluyó ejercicios de fortalecimiento). No se consideraron estudios de RT que no informaron variables de entrenamiento agudas de manera detallada y estudios que aplicaban ejercicios de fortalecimiento a ambos/todos los grupos (por ejemplo, que compararon dos tipos diferentes de entrenamiento de resistencia) no se consideraron. Solo se consideraron artículos totalmente revisados por pares con texto completo disponibles en inglés.
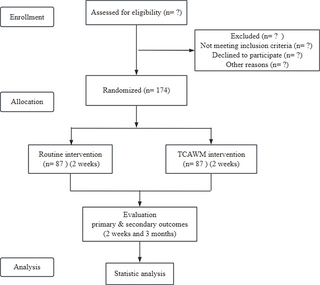
Selección de estudios
La búsqueda inicial fue realizada por un investigador (LR). Se seleccionaron títulos y resúmenes de publicaciones obtenidas por la estrategia de búsqueda y solo se eliminaron aquellos que obviamente estaban fuera del alcance de la revisión. Fuimos demasiado inclusivos en esta etapa y recibimos el texto completo para cualquier documento que potencialmente cumpliera con los criterios de inclusión de revisión. Siguiendo la detección del título/resumen, dos autores (LR, SII) los ensayos seleccionados independientemente para su inclusión; Según la información dentro de los informes completos, los ensayos elegibles se incluyeron en la revisión. Se recuperaron todos los juicios clasificados como elegibles por cualquiera de los autores. El desacuerdo entre los autores se resolvió mediante consenso o adjudicación de terceros (JTC, GKK).
Extracción y gestión de datos
Los datos fueron extraídos por dos autores de revisión utilizando un formulario personalizado (LR, JTC). Esto se utilizó para extraer datos relevantes sobre el diseño metodológico, los criterios de elegibilidad, las intervenciones (incluidas las características detalladas de los protocolos de entrenamiento), participantes, comparaciones y medidas de resultado. No había cegamiento para estudiar a autor, institución o revista en esta etapa.
Riesgo de sesgo
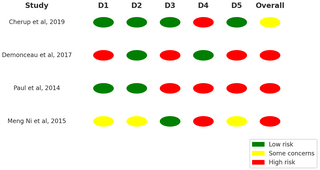
Para todos los estudios incluidos, la calidad metodológica fue evaluada por dos autores de forma independiente, utilizando la herramienta de riesgo de sesgo de Cochrane (32). Cada estudio se calificó para los siguientes dominios: generación de secuencias, ocultamiento de asignación, cegamiento (participantes y personal, evaluadores de resultados), datos de resultados incompletos e informes selectivos. Para cada estudio, los dominios se describieron como se informó en el informe de estudio publicado (o si es apropiado en función de la información de los protocolos relacionados, o los comentarios publicados) y juzgados por los autores de revisión en cuanto a su riesgo de sesgo de acuerdo con la Sección 8.5 del manual de Cochrane (33). Se les asignó una calificación de «bajo» si se cumplieron los criterios para un bajo riesgo de sesgo o se cumplían los criterios si se cumplían los criterios para un alto riesgo de sesgo. El riesgo de sesgo se consideró «poco claro» para un dominio, si no se informó detalle de lo que sucedió en el estudio, o si se conocía lo que sucedió en el estudio, pero el riesgo de sesgo era desconocido. Los desacuerdos entre los autores con respecto al riesgo de sesgo para los dominios se resolvieron por consenso.
Medidas del efecto del tratamiento
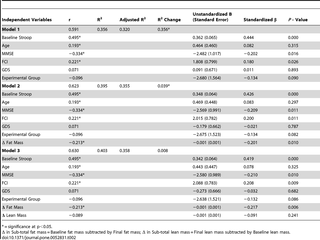
Para cada estudio, se calcularon las diferencias de medias (MD) o las diferencias de medias estandarizadas (SMD) y los intervalos de confianza del 95% (IC) para los resultados continuos utilizando el software Revman versión 5.2 de la colaboración Cochrane (34). Como se aconsejó en el Capítulo 7.7.3.1 y 9.4.5.2 del manual de Cochrane (33) Las estimaciones del efecto del tratamiento (MD, SMD) se basaron en comparaciones entre grupos utilizando datos posteriores a la intervención (comparación de valores finales entre los grupos). Cuando faltaban valores de datos continuos, se contactó a los autores del artículo. Hubo un caso en el que faltaban valores de desviación estándar (35) que se recuperaron después de la correspondencia con los autores. En el caso de que no hubiera evidencia de heterogeneidad del efecto (P> 0.1), se usó un modelo de efecto fijo para el metanálisis. En los casos en que hubo evidencia de heterogeneidad estadística, verificamos los resultados utilizando un modo de efectos aleatorios.
Evaluación de la heterogeneidad
La evaluación de la heterogeneidad entre los ensayos comparables se evaluó visualmente con el uso de parcelas forestales, así como las pruebas de chi² y las estadísticas de I², como se describe en el Capítulo 9.5 del manual de Cochrane (33). El nivel de importancia para la prueba de chi² se estableció en p = 0.1: se consideró que un valor p para chi² <0.1 indicó heterogeneidad estadísticamente significativa entre ...