1School of Family, Consumer, and Nutrition Sciences. Northern Illinois University, DeKalb, IL, Estados Unidos.
2Department of Kinesiology and Physical Education, Northern Illinois University, DeKalb, IL, Estados Unidos.
Resumen
INTRODUCCION
La carrera es una forma popular de realizar ejercicio en los Estados Unidos y muchos lo consideran un deporte de competición. Si bien las metas de rendimiento pueden ir desde simplemente finalizar una carrera hasta la competición en un evento olímpico, es probable que muchos participantes que buscan mejorar el rendimiento consuman diferentes suplementos nutricionales. Uno de los suplementos que recientemente ha cobrado interés como suplemento para mejorar el rendimiento físico es la beta-Alanina (βA) [1-10]. La βA es un aminoácido no proteico que se sintetiza en el hígado como metabolito final de la degradación del uracilo y de la timina. Si bien se sintetiza endógenamente, la fuente principal de βA en los seres humanos es la dieta. La carne es la fuente dietaria principal de βA, y las mayores concentraciones se encuentran en el pollo y en el pavo [11]. El potencial para aumentar el rendimiento de la suplementación con βA radica en su efecto sobre el aumento de los niveles de carnosina muscular [4, 7, 8, 12] debido a su rol como factor limitante en la síntesis de carnosina muscular [12-14].
La carnosina ((3-alanil-L-histidina) es un dipéptido que se encuentra en el tejido muscular y actúa como un amortiguador (buffer) intramuscular de [H+ ] [4, 7, 8, 12]. Durante el ejercicio de alta intensidad, la mayor dependencia de la glucólisis y del sistema de los fosfágenos para proporcionar ATP a los músculos activos, produce una acumulación de [H+ ], que provoca acidosis metabólica inducida por el ejercicio [15]. Una disminución en el pH ha sido señalada como causa de la fatiga muscular y de la disminución en la función contráctil del músculo [16]. Se cree que atenuando la acidosis inducida por el ejercicio se obtendrán aumentos en el rendimiento en actividades que requieren series prolongadas de trabajo de alta intensidad. Esta idea recibe el apoyo de resultados donde las concentraciones de carnosina en el músculo son más altas en esprinters [17], fisiculturistas [18] y atletas de deportes de equipo que participan regularmente en ejercicios intermitentes de alta intensidad [19, 20] que en sujtos sedentarios.
Estudios previos que investigaron el efecto de la βA en las mediciones de rendimiento han demostrado aumentos en el trabajo total realizado (TWD) [4, 10], el tiempo hasta el agotamiento (TTE) [1, 4, 10], la capacidad de trabajo físico en el umbral de fatiga (PWCFT) [1, 3], la producción de potencia en el umbral del lactato (LT) [5], la fatiga atenuada durante series repetidas de entrenamiento con sobrecarga [7] y el rendimiento en los 30 segundos finales de esprint durante una prueba contrarreloj de 2 horas [9]. Sin embargo las investigaciones han sido realizadas utilizado principalmente bicicletas ergométricas [1-5, 9, 10], por lo tanto es necesario determinar si la suplementación con βA ejerce un efecto ergogénico sobre el rendimiento en la carrera. Por consiguiente, planteamos la hipótesis que la suplementación con βA retrasaría el comienzo de la acumulación de lactato sanguíneo (OBLA). Por consiguiente, el propósito de este estudio fue determinar los efectos de 4 semanas de suplementación con βA sobre la relación HR-OBLA, % HR máx.-OBLA, % VO2 max-OBLA, y VO2 max durante una carrera incremental en cinta rodante.
METODOS
Sujetos
En el estudio participaron voluntariamente diecisiete varones activos recreacionalmente que corrían por lo menos 3 veces por semana y no habían consumido ningún suplemento deportivo durante por lo menos 6 semanas (Tabla 1). Los sujetos dieron su consentimiento informado por escrito para participar y todos los procedimientos del estudio fueron aprobados por el Comité de Revisión Institucional de la Universidad del Norte de Illinois, antes de comenzar el estudio.
Diseño Experimental
Este estudio usó un diseño experimental en doble ciego controlado con placebo de 2 tratamientos (pre vs post). En los días 1 y 29, los sujetos acudieron al laboratorio de ejercicio para la recolección de las mediciones antropométricas y para realizar un protocolo incremental de carrera en cinta rodante. Durante el estudio de 28 días, los sujetos fueron asignados al azar a un tratamiento donde consumían un suplemento que contenía βA (6,0 g.d-1) o un placebo (PL) de maltodextrina (6,0 g.d-1). En cada sujeto las evaluaciones Pre y Post-suplementación fueron realizadas en el mismo momento del día y con el mismo equipamiento. Se solicitó a los sujetos que ayunaran durante las 2 hrs previas a cada prueba. Se solicitó a los sujetos que se abstuvieran de consumir cualquier otro suplemento dietario y que mantuvieran su dieta regular y patrones de ejercicio durante todo el estudio. También se exigió a los sujetos abstenerse de consumir cafeína o realizar ejercicio vigoroso en las 24 hrs previas antes de los tests de ejercicios.
Los datos antropométricos fueron obtenidos con los sujetos vistiendo ropa deportiva y descalzos utilizando un estadiómetro montado en la pared y una balanza digital calibrada (Tanita Body Composition Analyzer TBF-300A, Tanita Corp, Arlington Heights, IL). Los sujetos fueron conectados a un sistema de medición del metabolismo automatizado (Parvomedics TrueMax 2400, Consentius Technologíes, Sandy, UT) mediante una boquilla y auricular; fueron conectados con un monitor telemétrico de frecuencia cardíaca (Polar F6, Finland) y permanecieron sentados para la determinación de las variables en reposo antes de las pruebas.
Los participantes realizaron 3 minutos de caminata en cinta rodante a 6,4 km.hr-1 (4,0 mph) para familiarizarse con el aparato. Luego la cinta rodante fue fijada a 9,6 km.hr-1 (6,0 mph) durante el tiempo de duración del test. Cada 3 minutos, la pendiente de la cinta rodante se incrementaba un 2%. Después de la etapa 5, todas las etapas restantes fueron realizadas con un aumento en la pendiente de 3% (etapas: 0%, 2%, 4%, 6%, 8%, 11%, 14%, 17%). La prueba continuó hasta que el participante alcanzaba el agotamiento volitivo. El consumo de oxígeno se obtuvo cada 30 segundos (s) a lo largo del test. El VO2 max se registró como el mayor promedio obtenido en 30 s alcanzado antes del agotamiento volitivo. El criterio para el VO2 max era haber alcanzado por lo menos dos o más de las siguientes condiciones: alcanzar una meseta (plateau) en el VO2 (aumento <2,1 mL.kg-1.min-1) las dos fases finales de la prueba, alcanzar una tasa de intercambio respiratorio (RER> 1,10) y/o alcanzar una HR dentro de 5 latidos.min-1 del valor máximo estimado para la edad (220-edad). En los 30 s finales de cada etapa, se solicitó a los participantes que informaran un índice de esfuerzo percibido (RPE) para todo el cuerpo, usando una escala numérica de 6-20 [21], la frecuencia cardíaca fue registrada y se recolectó una muestra de sangre capilar para determinación del lactato. Antes de iniciar el test, los sujetos fueron orientados con respecto al uso de la escala de RPE.
Un marcador fijo de 4,0 mmol.L-1 de sangre se utilizó para definir el comienzo de la acumulación de lactato en sangre (OBLA). Este valor fijo de lactato proporciona el análisis más razonable y preciso de lactato en relación con los objetivos del estudio y se ha demostrado que es una evaluación válida de los cambios fisiológicos, con especificidad sobre el rendimiento de resistencia [17] y mejoras en la aptitud física de resistencia [18].
Inmediatamente después de la recolección de datos de RPE y HR y faltando aún 30 s en cada etapa, mientras los sujetos todavía estaban corriendo se les solicitó que extendieran el dedo índice izquierdo, que fue preparado con un apósito con alcohol y secado con gasa. Después de la preparación, se realizó la punción de la yema del dedo con una lanceta y se recolectaron muestras de sangre en tubos capilares. Todas las muestras de lactato fueron analizadas inmediatamente por duplicado con un Analizador de Lactato Accutrend (F. Hoffman-La Roche S.A., Basilea, Suiza). Después de recopilar los datos, la etapa que produjo la concentración de lactato sanguíneo de 4,0 mmol.L-1 identificada previamente como OBLA [22] fue utilizada para determinar el umbral del lactato. OBLA, VO2max-OBLA y HR-OBLA fueron calculados utilizando interpolación lineal entre los puntos de datos relevantes, siguiendo la metodología descripta previamente por Neville et al. [23].
El protocolo en cinta rodante continuó hasta que se alcanzara el agotamiento volitivo y el valor más alto de frecuencia cardíaca alcanzada durante la prueba fue registrada como frecuencia cardíaca máxima (MHR). Luego también se identificó el OBLA por el porcentaje de la frecuencia cardíaca máxima en la cual se produjo (% HR máx.-OBLA).
Suplementación
Durante el estudio, se solicitó a los sujetos que se abstuvieran de consumir cualquier otro suplemento dietario y de realizar cambios en sus patrones dietarios o de ejercicio habituales. Los participantes fueron asignados al azar, siguiendo una metodología de aleatorización en doble ciego, a un grupo que consumía β-Alanina o a un grupo que consumía un Placebo. Los suplementos fueron proporcionados a los participantes en envases idénticos, sin marcas y sellados, y fueron proporcionados por Atheltic Edge Nutrition, Miami, Florida,. Los sujetos recibieron un suplemento de βA (6,0 g.d-1 βA, 600 mg N-Acetil-cisteína, 2,7 mg de ácido alfa-lipoico, 45 UI de Vitamina E) o un PL (maltodextrina de harina de arroz 6,0 g.d-1). Ambos grupos siguieron el mismo protocolo de suplementación de 3 cápsulas diarias repartidas en 3 tomas con las comidas.
Se ha demostrado que la suplementación con 6,4 g.d-1 de βA durante 28 días aumenta los niveles de carnosina en un 60% [4, 12], por lo que es posible asumir que los sujetos que consumieron el suplemento en este estudio experimentaron un aumento significativo en las concentraciones intramusculares de carnosina. Tres de los ocho sujetos en el grupo que consumió el suplemento con βA informaron que padecían hormigueo en sus dedos y manos. No se informó ningún otro efecto colateral en los individuos que consumieron el suplemento con βA y los sujetos del grupo PL no informaron efectos colaterales.
Análisis Estadísticos
Debido al grado en que los datos se apartaban de la distribución normal, no fue posible realizar una transformación de los mismos para obtener la normalidad estadística. Por esta razón, para analizar los datos, se utilizaron métodos estadísticos no paramétricos. Se utilizó el test de Friedman-para establecer las diferencias dentro de los grupos; y el test de Mann-Whitney para determinar las diferencias entre los grupos. Los datos fueron analizados con el software SPSS para Windows (Versión 16,0, 2007 Chicago, IL). Antes de comenzar el estudio el nivel de alfa para establecer la significancia estadística fue fijado en p<0,05. Los datos se presentan como Media±error estándar (SE).
RESULTADOS
Características de los Participantes
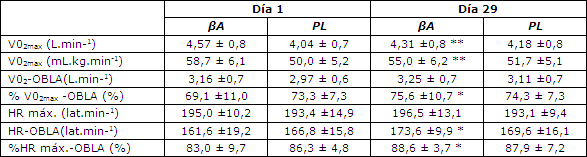
En el inicio del estudio (línea de base) no se observó ninguna diferencia en edad, talla, masa corporal, IMC, VO2 max absoluto L.min-1 (4,57±0,8 βA vs. 4,04±0,7 PL) VO2 max relativo ml.kg.min-1 (58,7±50,0 βA vs. 50,0 ± 5,2 PL) o frecuencia cardíaca máxima (HR máx.) lat.min-1 (195±10,2 βA vs. 193,4±14,9 PL) entre los sujetos en los dos grupos (Tabla 1). La Tabla 2 presenta los valores de la media y error estándar de VO2 max (L.min-1), VO2 max (ml.kg.min-1), % VO2 max – OBLA, VO2 – OBLA (lat.min-1) HR máx. (lat·min-1), HR-OBLA (lat·min-1), y % HR máx.-OBLA para ambos grupos de tratamientos antes (Pre) y después (Post) de los tests.
Tabla 1. Características físicas de los sujetos. Los datos se presentan en forma de Media ±SE.
En el día 1 pre-suplementación no se observó ninguna diferencia significativa en VO2 max entre los sujetos en los grupos βAy el PL (p = 0,154). En el día 29 (post-suplementación) los sujetos en el grupo que consumió βA experimentaron disminuciones significativas en los valores de VO2 max absoluto y relativo (p=0,005), pero en el grupo PL no se observaron cambios.
% VO2 max-OBLA
En el día 1 pre-suplementación no se observó ninguna diferencia significativa en el % VO2 max-OBLA entre los sujetos en los grupos βA y PL. En el día 29 (post-suplementación) los sujetos en el grupo que consumió βA presentaron un aumento significativo (p=0,034) en el % VO2 max-OBLA mientras que en el grupo PL no se observó ningún cambio.
Tabla 2. Parámetros de ejercicio pre- y post-suplementación. Los valores se expresan en forma de media±SE; *p<0,05 para los valores del grupo BA pre-Suplementación vs. valores del grupo BA post-suplementación. ** p<0,01 para los valores del grupo BA pre-suplementación vs. valores del grupo BA post-suplementación.
Frecuencia Cardíaca (HR) -OBLA y % HRmax-OBLA
El día 1 pre-suplementación no se observó ninguna diferencia significativa en la frecuencia cardíaca en OBLA (HR-OBLA), o en la frecuencia cardíaca porcentual máxima en OBLA (%HR máx.-OBLA) entre los sujetos en los dos grupos. En el día 29 (post-suplementación) los sujetos del grupo que consumió βA presentaron un aumento significativo (p=0,005) en HR-OBLA y % HRmax-OBLA (p=0,005), mientras que en el grupo que consumió el placebo no se observaron cambios. La relación HR – OBLA aumentó en 8 de los 8 sujetos que recibieron el suplemento de βA pero en el grupo placebo aumentó en 7 de los 9 sujetos, y en 2 de los 9 sujetos del grupo placebo se mantuvo sin cambios, después (post) y antes (pre) de la suplementación. El HRmax-OBLA porcentual aumentó en 7 de los 8 sujetos del grupo βA y disminuyó en 1 de los sujetos de este grupo, mientras que en el grupo PL aumentó en 6 de los 9 sujetos y disminuyó en 3 sujetos post versus pre suplementación.
Masa Corporal
Se observó un aumento estadísticamente significativo post-suplementación, en la masa corporal media en el grupo que consumió el suplemento con βA (p=0,034), mientras que no se observó ningún cambio en el grupo PL. La masa corporal media para el grupo βA aumentó 0,4 kg (77,9±9,0 a 78,3±9,3 kg) después del período de suplementación de 28 días, mientras que no se produjo ningún cambio en el grupo placebo (80,6±9,1 a 80,4±9,0 kg).
Índice de Masa Corporal (IMC)
Se observaron cambios en los valores del IMC pre vs. post-suplementación (p=0,034), siendo los valores pre-suplementación 23,7±2,3 en el grupo βA y 23,8±2,3 en el grupo PL y los valores post suplementación 24,9±1,8 para el grupo βA vs. 24,8±1,7 en el grupo PL.
Índice de Esfuerzo Percibido (RPE)
No se observaron cambios pre vs. post, en las puntuaciones finales del RPE obtenidas al finalizar la prueba en el grupo βA (18,50±0,42 a 17,50±0,82) versus el grupo de PL (18,56±0,44 a 18,78±0,32).
DISCUSION
Si bien los estudios previos han sugerido un efecto ergogénico de la suplementación con βA en ciclistas, éste fue el primer estudio en utilizar la carrera como protocolo de ejercicio. En éste estudio, los resultados demostraron que la suplementación con βA retarda el comienzo de la acumulación de lactato sanguíneo (OBLA) tal como se observa por los aumentos significativos en HR-OBLA, % HR máx. – OBLA en comparación con el grupo PL. Estos resultados son, en parte consistentes, con los de Zoeller et al. quienes observaron un aumento en la producción de potencia en el umbral del lactato en bicicleta ergométrica [5]. Estos investigadores no observaron ningún cambio en los parámetros ventilatorios (VO2 max en OBLA), sin embargo, es necesario señalar que Zoeller et al. utilizaron una dosis de βA de 3,2 g.d-1, mucho más baja que los 6,0 g.d-1 que utilizamos en este estudio [5].
Aunque en este estudio no se midieron los niveles musculares de carnosina, investigaciones previas han indicado que 4-10 semanas de suplementación con βA (2,4-6,4 g.d-1) incrementan 37-80% el nivel de carnosina en el músculo [4, 7, 8, 12] y que existe una relación significativa entre la concentración de carnosina y el rendimiento en ejercicio de alta intensidad [19]. Por otra parte, los niveles de carnosina son más altos en los atletas entrenados [20, 24, 25] y fisiculturistas [26] y se ha demostrado que aumentan en respuesta a los ejercicios de alta intensidad como en el entrenamiento de esprints [27].
Mecanismo Ergogénico de la Carnosina
Los individuos físicamente activos tienen concentraciones musculares de carnosina más altas que sus colegas sedentarios [20, 25-28] y está claro que tanto la suplementación con βA [4, 7, 8, 12] como el ejercicio de alta intensidad [28] aumentan independientemente los niveles de carnosina muscular. Aunque no se conoce todavía el mecanismo de acción exacto de la carnosina y el rendimiento, se han sugerido roles de la carnosina entre los que se incluyen por ej. que la misma actuaría como un antioxidante intramuscular [29], participaría en la regulación de la sensibilidad al calcio y en el par excitación-contracción (E-C) [30,31], brindaría protección contra la glucosilación actuando como un péptido sacrificatorio [32], y actuaría en la prevención de las uniones proteína-proteína reaccionando con los grupos carbonilos de las proteínas [33]. El mecanismo de acción más relevante para este estudio sería el papel de la carnosina como un buffer intramuscular para evitar la disminución del pH durante el ejercicio.
Efecto de la Suplementación con BA sobre la Cinética del Lactato
La cinética del lactato luego de la suplementación con βA ha sido analizada en tres estudios anteriores. Aunque el lactato no es la causa de la acumulación de [H+ ], el ambiente metabólico que causa una disminución en el pH también aumenta la producción de lactato, transformando al lactato en un buen marcador de las condiciones que inducen la acidosis metabólica [15]. Como sugirieron Van Thienen et al, un aumento en la capacidad buffer permitiría luna mejor producción de energía glucolítica y produciría un aumento global en la producción de lactato [9]. Sin embargo, estos investigadores no observaron un cambio significativo en la concentración de lactato sanguíneo luego de 30 s de esprint de ciclismo al finalizar una prueba contrarreloj de 110 minutos. Derave et al. tampoco pudieron observar diferencias en las concentraciones de lactato 90 y 180 s después de una carrera de 400 m entre el grupo A y el grupo PL [7]. De manera contraria, Zoeller et al., al evaluar la concentración de lactato durante aumentos incrementales en la intensidad de ejercicio en ciclismo, observaron un aumento en la producción de potencia (W) en el umbral del lactato [5]. Sin embargo, el VO2 max absoluto no cambió en el umbral de lactato.
Masa Corporal
La masa corporal aumentó en el grupo βA, pero en el grupo PL no se observó ningún cambio. Esto contradice estudios anteriores que reportaron que no se produjeron cambios en la masa corporal en respuesta a la suplementación con βA [4,8]. Smith et al., no observaron cambios en la masa corporal, pero observaron un aumento significativo en la masa corporal magra durante las primeras 3 semanas de suplementación (6g.d-1 de βA) junto con entrenamiento intervalado de alta intensidad [10]. Zoeller et al. informaron que la suplementación con βA o creatina solas no provocó aumentos en la masa corporal, pero en el grupo que consumió ambos suplementos, observaron un aumento en la masa corporal [5]. Hoffman et al. observaron que cuando los sujetos consumieron suplementos ya sea con placebo, creatina, βA, o creatina + βA, el grupo que consumió creatina + βA fue el que experimentó el mayor aumento en la masa corporal magra [6]. Autores de trabajos previos, han observado que los efectos propuestos de la suplementación con βA y el aumento en la masa corporal magra o masa corporal, se deben a una disminución en la acidosis junto con aumentos subsecuentes en el volumen de entrenamiento [6, 10].
Implicaciones de los Resultados del Estudio
Según nuestros conocimientos el presente estudio es el primero en analizar los efectos de βA en OBLA durante las fases incrementales de la carrera. Después de 28 días de suplementación con 6,0 g.d-1 de βA, el grupo de βA experimentó un retraso en OBLA tal como se observa por los aumentos en HR-OBLA y % HRmax-OBLA. Los resultados de este estudio son consistentes con los estudios discutidos previamente que observaron un retraso en la fatiga después de la suplementación con βA [1-5, 7, 9, 10]. Un retraso o desplazamiento hacia la derecha en OBLA durante un ejercicio de alta intensidad le da una ventaja significativa a un atleta que intenta mantener las contracciones musculares repetidas o prolongadas de alta intensidad. Además de los resultados de HR, también se observó un aumento en el % VO2 max-OBLA en el grupo de βA. Sin embargo, los autores creen que esto puede ser engañoso ya que también se observó una disminución en los valores de VO2 max luego de la suplementación en el grupo βA. Por consiguiente, el aumento en % VO2 max-OBLA simplemente puede deberse a una disminución en el valor del VO2 max. Esta disminución en VO2 max fue un resultado inesperado ya que es indicativo de una capacidad aeróbica reducida y no es una respuesta típica al entrenamiento.
Limitaciones
El suplemento usado en este estudio contenía antioxidantes adicionales (600 mg de N-Acetil-cisteína, 2,7 mg de ácido alfa lipoico, y 45 UI de Vitamina E) qué, por afirmaciones del fabricante, pueden colaborar sinérgicamente con el rol de la carnosina como antioxidante intramuscular. Sin embargo investigaciones previas sobre antioxidantes y ejercicios sugieren que un aumento aplicable del rendimiento debido a la actividad antioxidante es improbable [34-40]. Además, el mecanismo ergogénico sugerido previamente acerca de la carnosina no se basa en su función antioxidante, si no que en su participación como buffer intramuscular [19].
Se solicitó a los sujetos que no modificaran sus hábitos dietarios o de ejercicio durante los 28 días del estudio, que se abstuvieran de consumir cualquier otro suplemento dietético, que evitaran la cafeína o el ejercicio vigoroso durante por lo menos 24 hrs antes de la evaluación con ejercicios y que consumieran 3 píldoras diarias distribuidas en tres tomas con las comidas. La verificación de estos pedidos se limitó a la confirmación verbal por parte de los sujetos. Por consiguiente, podría ser posible que los individuos que consumieron el suplemento con βA estuvieran realizando ejercicios a una intensidad mayor y esto permitió el aumento significativo en la masa corporal. Además, si bien se utilizó una balanza Tanita para pesar a los sujetos, no se tomaron datos de la composición corporal. Por lo tanto el aumento en la masa corporal observado en este estudio, no puede ser diferenciado en masa corporal magra o masa grasa.
Conclusiones
Los resultados de este estudio sugieren que 28 días de suplementación con βA pueden aumentar el rendimiento de resistencia submáximo tal como se observó por la medición de OBLA. Los autores sugieren que la suplementación con βA puede haber optimizado la contribución relativa del sistema de energía anaeróbico pero también podría haber reducido la capacidad del sistema de energía aeróbico. Más específicamente, la demora en OBLA se basó en un mayor HR-OBLA y % HR máx.-OBLA en el grupo de individuos que consumieron la βA en comparación con el grupo que consumió el PL. Se necesitan investigaciones futuras para confirmar estos resultados y para evaluar variables racionadas al rendimiento, específicas de las carreras de fondo.
Investigaciones Futuras
Los estudios futuros deben centrarse en observar los efectos de βA en el rendimiento de carreras de 10-20 km que simulen ser carreras de resistencia de ruta. Con esto, debería considerarse un examen detallado del VO2 max. También sería interesante determinar los efectos ergogénicos de la βA en los deportes intermitentes, como el fútbol, hockey, básquetbol o fútbol americano que requieren una combinación de resistencia y rendimiento de esprint.
Intereses de Competencia
Los autores declaran que no poseen intereses de competencia.
Contribuciones de los autores
TJ fue el autor principal del manuscrito y desempeñó un papel importante en la recolección y análisis de los datos. JL, MM y JU tuvieron un papel importante en la recolección de los datos y preparación del manuscrito. Todos los autores han leído y han aprobado el manuscrito final.
Agradecimientos
A los autores les gustaría agradecer a Athletic Edge Nutrition 3109 Grand Avenue #280 Miami.FL http://www.aenutrition.com por donar los productos y 3000 dólares americanos para las mediciones de lactato. No se recibió ningún otro subsidio. Los autores desean agradecer al Dr. Paúl Luebbers, de la Universidad de Emporia State, por su ayuda editorial. La mención de cualquier ingrediente del suplemento dietético realizada en este trabajo no constituye un respaldo por parte de los autores.
Dirección para Envío de Correspondencia
Correo electrónico: [email protected]; School of Family, Consumer, and Nutrition Sciences. Northern Illinois; University, DeKalb, IL, Estados Unidos.
REFERENCIAS
1. Stout JR, Cramer JT, Mielke M, O'Kroy J, Torok D, Zoeller RF (2006). Effects of 28 days of beta-alanine and creatine monohydrate supplementation on the physical working capacity at neuromuscular fatigue threshold. J Strength Cond Res, 20(4):928-31
2. Stout JR, Cramer JT, Zoeller RF, Torok D, Costa P, Hoffman JR, Harris RC (2007). Effects of β-alanine supplementation on the onset of neuromuscular fatigue and ventilatory threshold in women. Amino Acids, 32(3):381-6
3. Stout JR, Graves BS, Smith AE, Hartman MJ, Cramer JT, Beck TW, Harris RC (2008). The effect of beta-alanine supplementation on neuromuscular fatigue in elderly (55-92 Years): a double-blind randomized study. J Int Soc Sports Nutr 2008, 5:21
4. Hill CA, Harris RC, Kim HJ, Harris BD, Sale C, Boobis LH, Kim CK, Wise JA (2007). Influence of b-alanine supplementation on skeletal muscle carnosine concentrations and high intensity cycling capacity. Amino Acids, 32:225-233
5. Zoeller RF, Stout JR, O'Kroy JO, TOrok D, Mielke M (2007). Effects of 28 days of beta-alanine and creatine monohydrate supplementation on aerobic power, ventilatory and lactate thresholds, and time to exhaustion. Amino Acids, 33(3):505-10
6. Hoffman J, Ratamess N, Kang J (2006). Effect of Creatine & β-alanine supplementation on performance and endocrine responses in strength/power athletes. Int J of Sport Nutr Exerc Metab, 4:430-6
7. Derave W, Ozdemir MS, Harris RC, Pottier A, Reyngoudt H, Koppo K, Wise JA, Achten E (2007). Beta-Alanine supplementation augments muscle carnosine content and attenuates fatigue during repeated isokinetic contraction bouts in trained sprinters. J Appl Physiol, 103(5):1736-43
8. Kendrick IP, Harris RC, Kim HJ, Kim CK, Dang VH, Lam TQ, Bui TT, Smith M, Wise JA (2008). The effects of 10 weeks of resistance training combined with beta-alanine supplementation on whole body strength, force production, muscular endurance and body composition. Amino Acids, 34(4):547-554
9. Van Thienen R, Van Proeyen K, Eynde B Vanden, Puype J, Lefere T, Hespel P (2009). Beta-alanine improves sprint performance in endurance cycling. Med Sci Sports Exerc, 41(4):898-903
10. Smith A, Walter A, Graef J, Kendall K, Moon J, Lockwood C, Fukuda D, Beck T, Cramer J, Stout J (2009). Effects of β-Alanine supplementation and high intensity interval training on endurance performance and body composition in men; a double-blind trial. J Int Soc Sports Nutr, 11:65-68
11. Abe H (2010). Role of histidine-related compounds as intracellular proton buffering constituents in vertebrate muscle. Biochemistry (Mosc) 65:757-65
12. Harris RC, Tallon MJ, Dunnett M, Boobis L, Coakley J, Kim HJ, Fallowfield JL, Hill CA, Sale C, Wise JA (2006). The absorption of orally supplied β-Alanine and its effect on muscle carnosine synthesis in human vastus lateralis. Amino Acids, 30:279-289
13. Bakardjiev A, Bauer K (1994). Transport of β-Alanine and biosynthesis of carnosine by skeletal muscle cells in primary culture. Eur J Biochem, 225:617-23
14. Dunnett M, Harris RC (1999). Influence of oral Beta-alanine and L-histidine supplementation on the carnosine content of the gluteus medius. Equine Vet J, 30:499-504
15. Robergs RA, Ghiasvand F, Parker D (2004). Biochemistry of exercise-induced metabolic acidosis. Am J Physiol Reul Integr Comp Physiol, 287:R502-R516
16. Messonnier L, Kristensen M, Juel C, Denis C (2007). Importance of pH regulation and lactate/H+ transport capacity for work production during supramaximal exercise in humans. J Appl Physiol, 102(5):1936-44
17. Nicolson RM, Sleivert GG (2001). Indices of lactate threshold and their relationship with 10-km running velocity. Med Sci Sports Exerc, 33(2):339-42
18. Jones AM, Doust JH (1998). The validity of the lactate minimum test for determination of the maximal lactate steady state. Med Sci Sports Exerc, 30:1304-13
19. Suzuki Y, Ito O, Mukai N, Takahashi H, Takamatsu K (2002). High level of skeletal muscle carnosine contributes to the latter half of exercise performance during 30-s maximal cycle ergometer sprinting. Jpn J Physiol, 52:199-205
20. Edge J, Bishop D, Goodman C (2006). The effects of training intensity on muscle buffer capacity in females. Eur J Appl Physiol, 96:97-105
21. Borg G (1970). Perceived exertion as an indicator of somatic stress. Scan J Rehab Med, 2(2):92-98
22. Neville V, Pain MTG, Folland JP (2009). Aerobic power and peak power of elite Americas Cup sailors. Eur J Appl Physiol, 106:149-157
23. Edge J, Bishop D, Hill-Haas S, Dawson B, Goodman C (2006). Comparison of muscle buffer capacity and repeated-sprint ability of untrained, endurance trained and team sport athletes. Eur J Appl Physiol, 96:225-234
24. Parkhouse WS, McKenzie DC, Hochachka PW, Ovalle WK (1985). Buffering capacity of deproteinized human vastus lateralis muscle. J Appl Physiol, 58:14-17
25. Tallon MJ, Harris RC, Boobis L, Fallowfield J, Wise JA (2005). The carnosine content of vastus lateralis is elevated in resistance trained bodybuilders. J Strength & Condit Res, 19:725-29
26. Suzuki Y, Ito O, Takahashi H, Takamatsu K (2004). The effect of sprint training on skeletal muscle carnosine in humans. Int J Sport Health Sci, 2:105-110
27. Begum G, Cunliffe A, Leveritt M (2005). Physiological role of carnosine in contracting muscle. Int J Sport Nutr Exerc Metab, 15(5):493-514
28. Boldyrev AA, Koldobski A, Kurella E, Maltseva V, Stvolinski S (1993). Natural histidine-containing dipeptide carnosine as a potent hydrophilic antioxidant with membrane stabilizing function. A biomedical aspect. Mol Chem Neuropathol, 19:185-92
29. Lamont C, Miller DJ (1992). Calcium sensitizing action of carnosine and other endogenous imidazoles in chemically skinned striated muscle. J Physiol, 454:421-34
30. Batrukova MA, Rubtsov AM (1997). Histidine-containing dipeptides as endogenous regulators of the activity of sarcoplasmic reticulum Carelease channels. Biochem Biophys Acta, 1324:142-150
31. Hipkiss AR, Michaelis J, Syrris P (1995). Non-enzymatic glycosylation of the dipeptide L-carnosine, a potential anti-protein-cross-linking agent. FEBS Lett, 371:81-85
32. Hipkiss AR (2000). Carnosine and protein carbonyl groups: a possible relationship. Biochemistry (Mosc), 65:771-778
33. Clarkson PM, Thompson HS (2000). Antioxidants: what role do they play in physical activity and health?. Am J Clin Nutr, 72(suppl):A637S-646SAm
34. Matuszczak Y, Farid M, Jones J (2005). Effect of n-acetylcysteine on glutathione oxidation and fatigue during handgrip exercise. Muscle Nerve, 32:633-638
35. Medved I, Brown MJ, Bjorksten AR (2003). N-acetylcysteine infusion alters blood redox status but not time to fatigue during intense exercise in humans. J Appl Physiol, 94:1572-1582
36. Bryant RJ, Ryder J, Martino P, Kim J, Craig BW (2003). Effects of vitamin E and C supplementation either alone or in combination on exercise-induced lipid peroxidation in trained cyclists. J Strength Cond Res, 17(4):792-800
37. Takanami Y, Iwane H, Kawai Y, Shimomitsu T (2000). Vitamin E supplementation and endurance exercise: are there benefits?. Sports Med, 29(2):73-83
38. Zoppi CC, Hohl R, Silva FC, Lazarim FL, Neto JM, Stancanneli M, Macedo DV (2006). Vitamin C and e supplementation effects in professional soccer players under regular training. J Int Soc Sports Nutr, 3:37-44
39. Gaeini AA, Rahnama N, Hamedinia MR (2006). Effects of vitamin E supplementation on oxidative stress at rest and after exercise to exhaustion in athletic students. J Sports Med Phys Fitness, 46(3):458-61
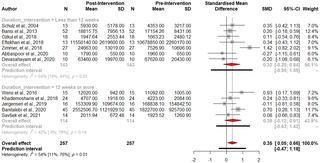
Aumento inducido por el ejercicio en el factor neurotrófico derivado del cerebro (BDNF) en personas con esclerosis múltiple: Una revisión sistemática y metaanálisis de ensayos de intervención de ejercicio
El papel del Factor Neurotrófico Derivado del Cerebro (BDNF) en la esclerosis múltiple (EM) ha...
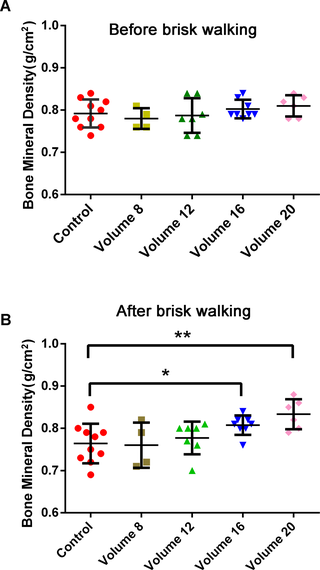
El volumen de caminata rápida es el factor clave para la mejora de la DMO en mujeres en premenopausia
Brisk Walking y Densidad Mineral Ósea: Clave para las Mujeres Premenopáusicas La osteoporosis es...
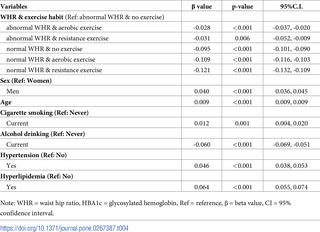
Efectos del ejercicio aeróbico y de resistencia en las concentraciones de hemoglobina glucosilada (HbA1c) en individuos taiwaneses no diabéticos según la relación cintura-cadera
El estudio analiza la relación entre los niveles de hemoglobina glucosilada (HbA1c) y la práctica...
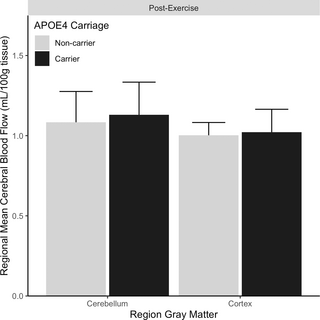
Riesgo de demencia y respuesta dinámica al ejercicio: Un ensayo clínico no randomizado
Resumen El ejercicio físico ha mostrado ser un aliado clave para la salud cerebral y la cognición...
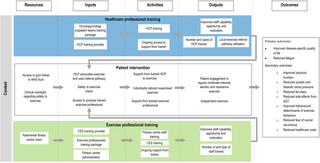
Evaluación del proceso para el ensayo controlado aleatorizado STAMINA: Un protocolo
Evaluación del Proceso del Ensayo Controlado Aleatorizado STAMINA Introducción El ensayo STAMINA...